 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知25℃时,0.01mol·dm-3HAc水溶液的解离度为4.2%,试计算:
已知25℃时,0.01mol·dm-3HAc水溶液的解离度为4.2%,试计算:
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知25℃时,0.01mol·dm-3HAc水溶液的解离度为4.2%,试计算:
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知25℃时,0.01mol·dm-3HAc水溶液的解离度为…”相关的问题
更多“已知25℃时,0.01mol·dm-3HAc水溶液的解离度为…”相关的问题
在298K时,浓度为0.01mol·dm-3的HAc溶液在某电导池中测得电阻为2220Ω.已知该电导池常数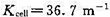 ,试求该条件下HAc的解离度和解离平衡常数。
,试求该条件下HAc的解离度和解离平衡常数。
A.渗透浓度为40mmol·L-1NaCl
B.渗透浓度为10mmol·L-1Na3PO4
C.渗透浓度为400mmol·L-1Na3PO4
D.0.02mol·L-1Na2CO3
298K时,在Ag+/Ag电极中加入过量I-,设达到平衡时c(I-)=0.1mol·dm-3,而另一电极为Cu2+/Cu,c(Cu2+)=0.01mol·dm-3,将两电极组成原电池,写出原电池符号、电池反应,并求电池反应平衡常数。
已知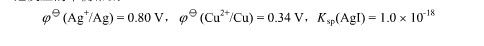
以过氧化二特丁基在60℃下引发苯乙烯在苯溶液中聚合,引发剂浓度为0.01mol·L-1,单体浓度为1.0mol·L-1,测得初期聚合速率Rp为1.5×10-7mol·L-1·s-1,相对分子质量为104000。已知60℃时苯乙烯的kt=3.6×107L·mol-1·s-1,f=0.9。试求: 总速率常数?
298K时,已知 (NaCl)=1.086×10-2S·m2·mol-1,-2(NaOH)=2.172×10-2S·m2·mol-1和
(NaCl)=1.086×10-2S·m2·mol-1,-2(NaOH)=2.172×10-2S·m2·mol-1和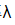 (NH4Cl)=1.298×10-2S·m2·mol-1;NH3·H2O在浓度为0.1mol·dm-3时的摩尔电导率Am=3.09×10-4S·m2·mol-1,浓度为0.01mol·dm-3时的摩尔电导率Am=9.62×10-4S·m2·mol-1。试根据上述数据求NH3·H2O的两种不同浓度溶液的解离度和解离常数。
(NH4Cl)=1.298×10-2S·m2·mol-1;NH3·H2O在浓度为0.1mol·dm-3时的摩尔电导率Am=3.09×10-4S·m2·mol-1,浓度为0.01mol·dm-3时的摩尔电导率Am=9.62×10-4S·m2·mol-1。试根据上述数据求NH3·H2O的两种不同浓度溶液的解离度和解离常数。
A.100%;
B.99%;
C.1.0%;
D.0.0%。
A.下列溶液沸点最高的是
B.0.01mol/L的蔗糖溶液
C.0.01mol/L的MgCl2溶液
D.0.02mol/L的H2S溶液
E.0.02mol/L的NaNO3溶液
A.0.01mol· Lˉ 1蔗糖溶液
B.0.01mol· Lˉ 1CaC12溶液
C.0.02mol· Lˉ 1NaCl溶液
D.0.02mol· Lˉ 1CH3COOH溶液