 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在298K时,浓度为0.01mol·dm-3的HAc溶液在某电导池中测得电阻为2220Ω.已知该电导池常数 ,试求
在298K时,浓度为0.01mol·dm-3的HAc溶液在某电导池中测得电阻为2220Ω.已知该电导池常数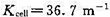 ,试求该条件下HAc的解离度和解离平衡常数。
,试求该条件下HAc的解离度和解离平衡常数。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在298K时,浓度为0.01mol·dm-3的HAc溶液在某电导池中测得电阻为2220Ω.已知该电导池常数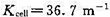 ,试求该条件下HAc的解离度和解离平衡常数。
,试求该条件下HAc的解离度和解离平衡常数。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在298K时,浓度为0.01mol·dm-3的HAc溶液在某…”相关的问题
更多“在298K时,浓度为0.01mol·dm-3的HAc溶液在某…”相关的问题
298K时,在Ag+/Ag电极中加入过量I-,设达到平衡时c(I-)=0.1mol·dm-3,而另一电极为Cu2+/Cu,c(Cu2+)=0.01mol·dm-3,将两电极组成原电池,写出原电池符号、电池反应,并求电池反应平衡常数。
已知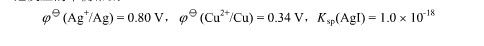
在298K和标准压力时,电解一含Zn2+溶液,希望当Zn2+浓度降至1×10-4mol·kg-1时,仍不会有H2(g)析出,试问溶液的pH值应控制在多少为好?已知H2(g)在Zn(s)上的超电势为0.72V,并设此值与溶液浓度无关。
A.渗透浓度为40mmol·L-1NaCl
B.渗透浓度为10mmol·L-1Na3PO4
C.渗透浓度为400mmol·L-1Na3PO4
D.0.02mol·L-1Na2CO3
已知298K时浓度为0.010mol·L-1的某一元弱酸溶液的pH为4.00,则该酸的解离平衡常数Ksp约为______;将该溶液稀释后,其pH将变______,解离度α将变______,其将______。
在298K时,某溶液含MgCl2和ZnSO4的浓度均为0.002mol·kg-1,试用Debye-Htickel极限公式求ZnSO4的离子平均活度因子。
A.1mol/L
B.2mol/L
C.0.1mol/L
D.0.01mol/ml
初浓度对反应时间的影响
设某反应的动力学方程
已知电对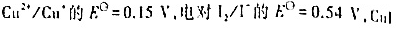 的
的
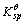 =1.3×10-12。
=1.3×10-12。
(1)试求氧化还原反应
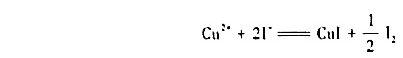
298K时的平衡常数;
(2)若溶液中Cu2+的起始浓度为0.10 mol·dm-3,I-的起始浓度为1.0 mol·dm-3,试计算达到平街时留在溶液中Cu2+的浓度。