 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知298K时浓度为0.010mol·L-1的某一元弱酸溶液的pH为4.00,则该酸的解离平衡常数约为______;将该溶液稀释后
已知298K时浓度为0.010mol·L-1的某一元弱酸溶液的pH为4.00,则该酸的解离平衡常数Ksp约为______;将该溶液稀释后,其pH将变______,解离度α将变______,其将______。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知298K时浓度为0.010mol·L-1的某一元弱酸溶液的pH为4.00,则该酸的解离平衡常数Ksp约为______;将该溶液稀释后,其pH将变______,解离度α将变______,其将______。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知298K时浓度为0.010mol·L-1的某一元弱酸溶液…”相关的问题
更多“已知298K时浓度为0.010mol·L-1的某一元弱酸溶液…”相关的问题
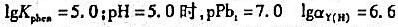 )
)
已知Fe3+与EDTA配合物的lgKFeY=25.1,若在pH=6.0时以0.010mol/L EDTA滴定同浓度的Fe3+,考虑αY(H)和αFe(OH)后,lg
已知电对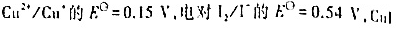 的
的
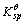 =1.3×10-12。
=1.3×10-12。
(1)试求氧化还原反应
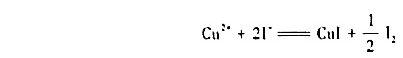
298K时的平衡常数;
(2)若溶液中Cu2+的起始浓度为0.10 mol·dm-3,I-的起始浓度为1.0 mol·dm-3,试计算达到平街时留在溶液中Cu2+的浓度。
298K时,用0.1000mol/LNaOH溶液滴定20.00mL同浓度的甲酸溶液过程中溶液PH与NaOH溶液体积的关系如图所示(已知:HCOOH溶液的Ka=l.0×10-4.0),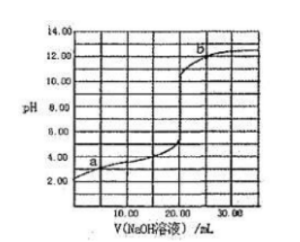 下列有关叙述正确的是()。
下列有关叙述正确的是()。
A.该滴定过程应该选择甲基橙作为指示剂
B.图中a,b两点水的电离程度:b>a
C.当加入10.00mLNaOH溶液时,c(HCOO-)>c(H+)>c(Na+)>c (OH-)
D.当加入20.00mLNaOH溶液时,溶液pH>8.0
A.1.0×10-4mol·L-1
B.1.0×10-7mol·L-1
C.0.10mol·L-1
D.1.0X10-12mol·L-1
A.[H3PO4]〈0.010mol·dm-3
B.[H2PO- 4]〉[HPO2- 4]
C.[H+]〉0.010mol·dm-3
D.[OH-]〉[PO3- 4]
已知反应:

298K时的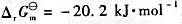 。试计算:
。试计算:
(1)该反应的标准平衡常数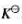 ;
;
(2)若空气中H2S的分压为3.1Pa,试计算可以确保铜单质免遭H2S腐蚀时H2的分压。