 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
100mL 0.100mol/L HA弱酸溶液,用25.0mL乙醚萃取,萃取后取出25.0mL水相,需20.0mL0.0500mol/L NaOH溶液与之中
和,计算HA在有机相与水相中的比值为多少?
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“100mL 0.100mol/L HA弱酸溶液,用25.0m…”相关的问题
更多“100mL 0.100mol/L HA弱酸溶液,用25.0m…”相关的问题
A.200
B.300
C.150
D.250
准确量取30.00ml弱酸,加水稀释至100ml。以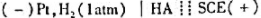 为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
(1)弱酸HA的Ka。
(2)原弱酸HA的浓度。
A.1.0×10-6mol/L
B.1.0×10-7mol/L
C.1.0×10-8mol/L
D.1.0×10-9mol/L
A.流感病毒属正粘病毒科,单股、正链 、分节段RNA病毒
B.可呈球状和丝状
C.囊膜上糖蛋白包括血凝素HA、神经氨酸酶NA和M1蛋白
D.对外界抵抗力弱,可被乙醇、碘酊、紫外线等灭活
A.9.26
B.4.47
C.7.00
D.10.00
某弱酸HA总浓度为2.0×10-4mol/L。于λ520nm处,用1cm比色皿测定,在不同pH值的缓冲溶液中,测得吸光度值如下:
| pH | 0.88 | 1.17 | 2.99 | 3.41 | 3.95 | 4.89 | 5.50 |
| A | 0.890 | 0.890 | 0.692 | 0.552 | 0.385 | 0.260 | 0.260 |
求:
A.该溶液的pH=4
B.升高温度,溶液的pH增大
C.此酸的电离平衡常数约为1×10-7
D.由HA电离出的c(H+)约为水电离出的c(H+)的1000000倍