 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知25°C时AgBr的活度积Kap=4.88x10-13,,.试计算25℃时 (1)银-溴化银电极的标准
已知25°C时AgBr的活度积Kap=4.88x10-13,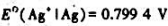 ,
,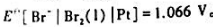 .试计算25℃时
.试计算25℃时
(1)银-溴化银电极的标准电极电势Eθ[Br-|AgBr(s)|Ag];
(2)AgBr(s)的标准摩尔生成吉布斯函数.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知25°C时AgBr的活度积Kap=4.88x10-13,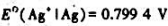 ,
,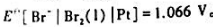 .试计算25℃时
.试计算25℃时
(1)银-溴化银电极的标准电极电势Eθ[Br-|AgBr(s)|Ag];
(2)AgBr(s)的标准摩尔生成吉布斯函数.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知25°C时AgBr的活度积Kap=4.88x10-13,…”相关的问题
更多“已知25°C时AgBr的活度积Kap=4.88x10-13,…”相关的问题
25℃时,AgCI的溶度积K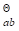 =1.71×10-10,试求在饱和水溶液中.AgCI的离子平均活度及离子平均活度系数各为多少?
=1.71×10-10,试求在饱和水溶液中.AgCI的离子平均活度及离子平均活度系数各为多少?
25℃下测得CS2(B)和丙酮(C)形成的混合溶液在不同浓度时CS2(B)的分压为

已知CS2的亨利系数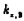 =267.98kPa,请分别用拉乌尔定律计算CS2的活度与活度因子,并讨论结果说明了什么.
=267.98kPa,请分别用拉乌尔定律计算CS2的活度与活度因子,并讨论结果说明了什么.
[Cu(NH3)4]2+溶液等体积混合,有无Cu(OH)2沉淀生成?[已知Cu(OH)2的Kapθ=2.2X10-20]
298K时,有电池Pt|H2(100kPa)|HI(m)|AuI(S)|Au(s)。 (1)请写出各电极反应及电池反应。 (2)m=1×10-4mol/kg时,电动势E=0.97V;若m=3.0mol/kg时,E=0.41V。求m=3.0mol/kg时,HI的平均活度系数。 (3)已知Au+(aq)+e-→Au(8)的φΘ=1.68V,求AuI的溶度积。
在25℃下将铁放入Fe2+活度为1的溶液(pH=3)中,已知Fe2+还原为Fe的交换电流密度为2×10-5A·m-2,氢在该溶液中析出的交换电流密度为1.6×10-3A·m-2;Fe氧化过程和氢离子还原过程的b值分别为0.06和0.12V,试求腐蚀电位和腐蚀电流密度。
25℃时,某电解质溶液中含有的阳离子为Ag+(α=0.05)、Cd2+(α=0.001)、Ni2+(α=0.1)和H+(α=0.001)。若用Pt电极电解此溶液,则当外加电压从零开始逐渐增加时,分析在阴极上依次析出的物质。已知H2(g)在Pt、Ag、Cd及Ni上的超电势分别为0.12、0.20、0.30及0.24V。假设在Pt等金属上析出上述各种金属的超电势可忽略不计,H+的活度不随电解的进行而变化,析出的H2压力为101.325kPa。
A.=0.1036
B.=15.32
C.=0.16445
D.无法确定