 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
如图中所示,将纯物质沿气-液饱和线升温。当到达图中点C时,()的分界面消失,体系的性质变得无一。
A.固
B.气
C.液
D.超临界态
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.固
B.气
C.液
D.超临界态
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“如图中所示,将纯物质沿气-液饱和线升温。当到达图中点C时,(…”相关的问题
更多“如图中所示,将纯物质沿气-液饱和线升温。当到达图中点C时,(…”相关的问题
工业上以锂辉石(Li2O·A12O3·4SiO2,含少量Ca、Mg元素)为原料生产碳酸锂。其部分工艺流程如下: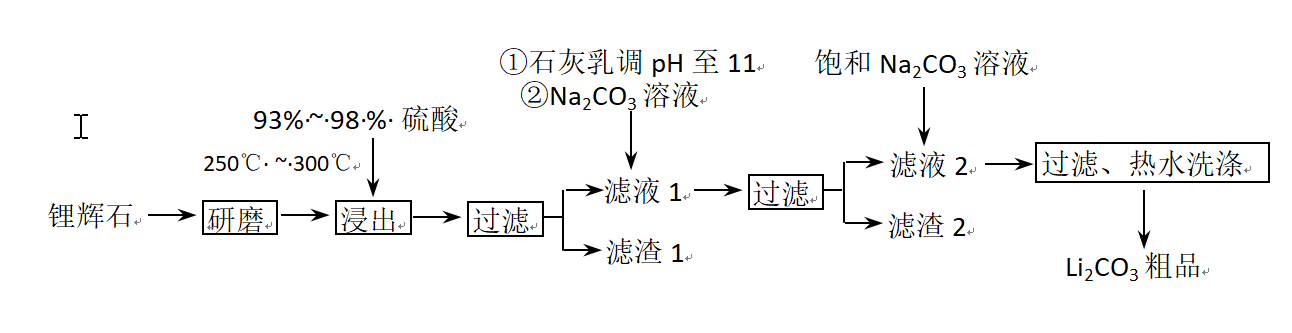 已知:①
已知:①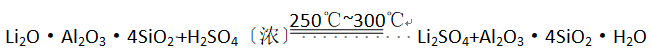 ②某些物质的溶解度(S)如下表所示
②某些物质的溶解度(S)如下表所示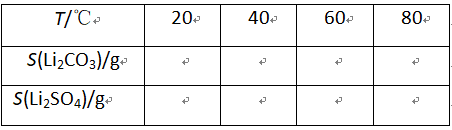
问题一、从滤渣1中别离出Al2O3的部分流程如以下图所示,括号表示加入的试剂,方框表示所得到的物质。则步骤Ⅱ中反应的离子方程式是()。
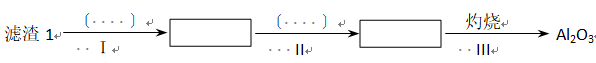
问题二、已知滤渣2的主要成分有Mg(OH)2和CaCO3向滤液1中加入石灰乳的作用是(运用化学平衡原理简述)()
问题三、向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是()
问题四、工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下()
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解
b.电解后向LiOH溶液中加入过量NH4HCO3溶液,过滤、烘干得高纯Li2CO3
①a中,阳极的电极反应式是()。
②b中,生成Li2CO3反应的化学方程式是()。
具有饱和非线特性的非线性控制系统如图8-17所示,若r(t)=0,试在e一
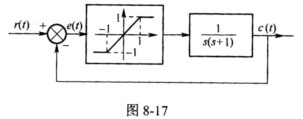 平面上绘制e(0)=2,
平面上绘制e(0)=2,
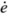 (0)=0时的相轨迹图(要求将解题过程写清楚)。
(0)=0时的相轨迹图(要求将解题过程写清楚)。
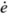

A.制冷剂R22和R410A的制冷剂状态可以在一张压焓图中表示
B.压焓图中可以读取制冷的温度、压力、比容、焓、熵、湿度等六个状态参数
C.压焓图中的焓值是指制冷剂的能量状态,物质对外做功焓值降低,吸收热量焓值增加
D.制冷剂的六个状态参数中,任意知道两个状态参数,就可以确定制冷剂的状态
E.压焓图中饱和液体线与饱和蒸汽线是制冷剂过冷液体区、气液两相区、过热蒸汽区三个区的分界线
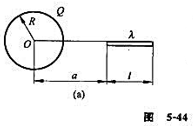
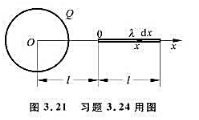
如图 5-44(a)所示,半径为R的均勾带电球面,带有电荷Q,沿某一半径方向上有一均匀带电细线,电荷线密度为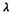 ,长度为I,细线左端离球心距离为a.设球和线上的电荷分布不受相互作用影响,试求细线所受球面电荷的电场力和细线在该电场中的电势能(设无穷远处的电势为零)。
,长度为I,细线左端离球心距离为a.设球和线上的电荷分布不受相互作用影响,试求细线所受球面电荷的电场力和细线在该电场中的电势能(设无穷远处的电势为零)。
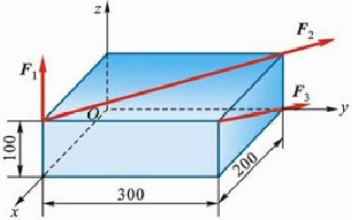
力系中,F1=100N,F2=300N,F3=200N,各力作用线的位置如图4-5所示。将力系向原点O简化 。
由组分A与B组成的溶液,液相活度系数与组成的关联式为: ,已知90℃时,纯物质的饱和蒸气压分别为
,已知90℃时,纯物质的饱和蒸气压分别为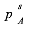 =133.289kPa,
=133.289kPa,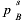 =93.303kPa,系统符合低压气液平衡的关系式,试求:
=93.303kPa,系统符合低压气液平衡的关系式,试求:
如图8—2所示,将一锲形铜片置于间距恒定的两轧辊间轧制。
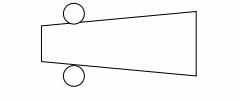
①分析轧制后铜片经再结晶后晶粒大小沿片长方向变化。
②如果在较低温度下退火,何处先发生再结晶?为什么?