 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列各组溶液中,能以一定体积比组成缓冲溶液的是()
A.浓度均为0. 1 mol/L的NaAc溶液和HAc溶液
B.浓度均为0. 1 mol/L的NaOH溶液和HCl溶液
C.浓度均为0. 1 mol/L的NaOH溶液和NH3溶液
D.浓度均为0. 1 mol/L的HAc溶液和HCl溶液
E.浓度均为0. 1 mol/L的NaOH溶液和H2SO4溶液
 答案
答案
A、浓度均为0. 1 mol/L的NaAc溶液和HAc溶液
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.浓度均为0. 1 mol/L的NaAc溶液和HAc溶液
B.浓度均为0. 1 mol/L的NaOH溶液和HCl溶液
C.浓度均为0. 1 mol/L的NaOH溶液和NH3溶液
D.浓度均为0. 1 mol/L的HAc溶液和HCl溶液
E.浓度均为0. 1 mol/L的NaOH溶液和H2SO4溶液
 答案
答案
A、浓度均为0. 1 mol/L的NaAc溶液和HAc溶液
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列各组溶液中,能以一定体积比组成缓冲溶液的是()”相关的问题
更多“下列各组溶液中,能以一定体积比组成缓冲溶液的是()”相关的问题
A.要除去氯化镁溶液中少量的氯化铁,可以向溶液中加入适当的氢氧化钠溶液
B.向含有碳酸镁固体的溶液中滴加少许浓盐酸(忽略体积变化),C(CO32-)变小
C.在同浓度的盐酸中,ZnS可溶而CuS不溶,说明CuS的溶解度比ZnS的小
D.向氯化银,溴化银的饱和溶液中加入少量硝酸银,溶液中C(I-):C(Br-)不变
A.0.10mol·L-1NH3·H2O溶液和0.10mol·L-1NH4Cl溶液等体积混合后的溶液
B.0.20mol·L-1NH3·H2O溶液和0.20mol·L-1NH4Cl溶液等体积混合后的溶液
C.0.20mol·L-1NH3·H2O溶液和0.20mol·L-1NH4Cl溶液以体积比2:1混合后的溶液
D.0.20mol·L-1NH3·H2O溶液和0.10mol·L-1NH4Cl溶液等体积混合后的溶液
由一元弱酸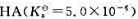 和它的共轭碱NaA组成的缓冲溶液中,HA的浓度为0.25mol·L-1.若在100mL此缓冲溶液中加入5.0mmolNaOH固体,溶液的pH变为5.60。计算加入NaOH固体前缓冲溶液的pH.
和它的共轭碱NaA组成的缓冲溶液中,HA的浓度为0.25mol·L-1.若在100mL此缓冲溶液中加入5.0mmolNaOH固体,溶液的pH变为5.60。计算加入NaOH固体前缓冲溶液的pH.
A.50g溶质质量分数为2%的碘酒中含有1g碘
B.10g食盐溶液中溶质质量分数一定比5g食盐溶液中溶质质量分数大
C.将一杯溶质质量分数为20%的食盐水倒出一半,则剩余溶液的溶质质量分数为10%
D.溶质质量分数为10%的食盐溶液是指100g 水中溶解了l0g食盐
A.乙酸能以任意比混溶
B.乙酸能与碳酸钠溶液反应产生二氧化碳
C.1mol/L的乙酸能使紫色的石蕊试液变红色
D.乙酸能与乙醇反应生成乙酸乙酯
A.CH3C00H与水能以任意比混溶
B.CH3C00H能与NA2CO3溶液反应,产生C02气体
C.1mol/L的CH3C00H水溶液能使紫色石蕊试液变红
D.1mol/L的CH3C00Na溶液的PH约为9
A.混合物中一定不含有Na2CO3、NaCl
B.混合物中一定有Na2O2、NaHCO3
C.无法确定混合物中是否含有NaHCO3
D.混合物中一定不含Na2O2、NaCl
A.10mL水和10mL酒精混合能得到小于20mL混合溶液,说明水分子体积比酒精分子小
B.加压25m3的石油气可装入容积为0.24m3钢瓶中,说明气体分子间有一定的间隔
C.糖块放进水中后,很快消失,说明蔗糖分子分解成了更小的粒子
D.物体的热胀冷缩现象,是物质分子总是在不断运动的缘故
A.中和同体积同浓度的HAc和HCl,所需碱量是相同的
B.由H2CO3的解离平衡,可知溶液中H+]和CO32-]的比值=2∶1
C.血液中HCO3-]和CO32-]的比值达到20/1,但由呼吸作用和肾的生理功能的补充或调节,使HCO3-和CO2溶解的浓度保持相对稳定而使血浆中的碳酸缓冲系具有缓冲能力
D.缓冲容量β越大,溶液的缓冲能力越强
pH玻璃电极与饱和甘汞电极组成如下电池:玻璃电极|H+(x)‖饱和甘汞电极。测定pH为4.01的邻苯二甲酸氢钾缓冲溶液时,其电池电动势为0.211V。而测定两个未知溶液时,其电池电动势分别为0.435V和0.0186V,试计算两种未知溶液的pH(25℃)。