 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知:H2(g)+F2(g)====2HF(g) ΔH=-546.6 kJ•mol-1,下列说法中不正确的是()
A.44.8 L氟化氢气体分解成22.4 L的氢气和22.4 L的氟气吸收546.6 kJ热量
B.1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量大于546.6 kJ
C.相同条件下,1 mol氢气与1 mol氟气的能量总和高于2 mol氟化氢气体的能量
D.2 mol H—F键的键能比1 mol H—H键和1 mol F—F 键的键能之和大546.6 kJ
 答案
答案
A、44.8 L氟化氢气体分解成22.4 L的氢气和22.4 L的氟气吸收546.6 kJ热量
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案

 更多“已知:H2(g)+F2(g)====2HF(g) ΔH=-5…”相关的问题
更多“已知:H2(g)+F2(g)====2HF(g) ΔH=-5…”相关的问题
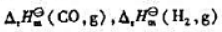
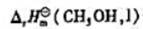 计算该反应的
计算该反应的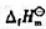 .
.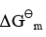
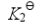
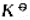 =0.618.若系统中各组分气体分压为p(CO2)=p(H2)=127kPa,p(CO)=p(H2O)=76kPa,计算此时
=0.618.若系统中各组分气体分压为p(CO2)=p(H2)=127kPa,p(CO)=p(H2O)=76kPa,计算此时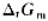 (973K)时值并判断反应进行的方向。
(973K)时值并判断反应进行的方向。
















