 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
把空气作为理想气体,当其中O2的质量分数为21%,N2的质量分数为78%,其他气体的质量分数为1%,则其定压比热容c为()J/(kg。K)。
A.707
B.910
C.1010
D.1023
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.707
B.910
C.1010
D.1023
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“把空气作为理想气体,当其中O2的质量分数为21%,N2的质量…”相关的问题
更多“把空气作为理想气体,当其中O2的质量分数为21%,N2的质量…”相关的问题
A.热力学研究方法全部有效
B.(1)(2)(3)(5)能适用
C.只有(1),其它都不适用
D.(1)(2)(5)能适用
A.N2
B.O2
C.H2O
D.O2
A.加入稀盐酸后一定没有气泡产生
B.该CaO样品的成分可能是CaO和Ca(OH)2
C.生成CaCl2的质量为11.1 g
D.该CaO样品的成分可能是Ca(OH)2和 CaCO3
A.①在恒温的条件下,将足量的氯化钠饱和溶液蒸发适量的水分
B.②向露置在空气中部分变质的氢氧化钠溶液中加入稀盐酸
C.③向氢氧化钠溶液中不断加水稀释
D.④质量相同且过量的锌粉和铁粉,分别与质量和质量分数相同的稀盐酸反应
A.酒精既可作溶剂,也可作溶质
B.酒精与空气接触即可燃烧
C.酒精由三种元素组成,其中碳元素的质量分数最大
D.酒精属于有机物,完全燃烧后的产物为二氧化碳和水
烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点。
问题一、选择性催化复原法的脱硝原理为:

①上述反应中每转移3mol电子,生成标准状况下N2的体积为()L。
②已知:2H2(g)+O2(g)=2H2O(g)ΔH=-483.6kJ•mol-1
N2(g)+3H2(g)=2NH3(g)ΔH=-92.4kJ•mol-1
N2(g)+O2(g)=2NO(g)ΔH=-180.5kJ•mol-1
则反应6NO(g)+4NH3(g)=5N2(g)+6H2O(g)的ΔH=()。
问题二、目前,科学家正在研究一种以乙烯作为复原剂的脱硝(NO)原理,其脱硝机理示意图如以下图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示。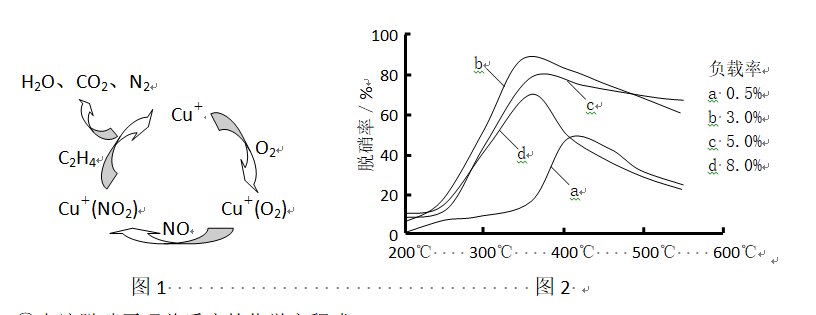
①出该脱硝原理总反应的化学方程式:()。
②为到达最正确脱硝效果,应采取的条件是()。
A.已知A+B==C将agA和bgB在适当条件下充分反应后,分析得知最后剩余物为纯净物,则生成物C的质量等于(a+b)g
B.物质在空气中加热发生反应后,生成各物质的总质量必定等于参加反应各物质的总质量
C.60的独特结构决定有可能广泛应用于超导、催化、材料、医学及生物等领域
D.当空气中二氧化碳的质量分数为1%,会使人神志不清、呼吸停止,以致死亡
A.熔点:戊烷>2,2一二甲基戊烷>2,3一二甲基丁烷>丙烷
B.密度:CHCl3>H2O>己烷
C.氢元素质量分数:甲烷>乙烷>乙烯>乙炔(C2H2)>苯
D.等质量物质完全燃烧耗O2量:苯>环己烷(C6H12)>己烷
A.热量可以自发地从高温物体传到低温物体
B.第二类永动机不能制成,因为它违反了能量守恒定律
C.一定质量的理想气体在等温膨胀过程中,从外界吸收的热量全部用来做功,这一过程违反了热力学第二定律
D.当把打足气的车胎内的气体迅速放出时,会发现气嘴处的温度明显降低,这是因为气体对外做功,胎内气体温度降低