 更多“()小明和小红分别给电池标注了正极和负极,他们的标注正确吗”相关的问题
更多“()小明和小红分别给电池标注了正极和负极,他们的标注正确吗”相关的问题
A.锌为正极,Ag2O为负极
B.原电池工作时,负极区PH增大
C.原电池工作时,负极区PH增大,正极区PH减小
D.锌为负极:Zn+2OH--2e- =ZnO+H2O
A.充电时的总反应为FePO4+Li===LiFePO4
B.充电时动力电池上标注+的电极应与外接电源的正极相连
C.放电时电池内部Li+向负极移动
D.放电时,在正极上是Li+得电子被还原
A.正极发生还原反应
B.正极与负极上参加反应的气体的物质的量之比为 2∶9
C.通乙烷的电极为负极
D.电池工作过程中,溶液的 pH 逐渐减小
A.红色表笔接电池负极,黑色表笔接电池正极
B.红色表笔接电池正极,黑色表笔接电池负极
C.红表笔和黑表笔都接电池正极
D.红表笔和黑表笔都接电池负极
A.红色表笔接电池负极,黑色表笔接电池正极
B.红色表笔接电池正极,黑色表笔接电池负极
C.红表笔和黑表笔都接电池正极
D.红表笔和黑表笔都接电池负极
A.电池工作时,CO32-向负极移动
B.电池放电时,电子经外电路由通氧气的正极流向通氢气的负极
C.正极的电极反应式为4OH- - 2e- = O2↑+2H2O
D.通氧气的电极为正极,发生氧化反应
A.电池正极接电源正极,电池负极接电源负极
B.电池正极接电源正极,电池负极接电源正极
C.电池正极接电源负极,电池负极接电源负极
D.电池正极接电源负极,电池负极接电源正极
电池反应S2O32-(aq)+2OH-(aq)+O2(g)===2SO32-(aq)+H2O(1)的Eθ为0.98 V,则正极反应为________________,负极反应为________________,若Eθ(O2/H2O)=0.40 V,则Eθ(SO32-S2O32-)=________________。
如图是2004年批量产生的笔记本电脑所用甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为:2CH3OH+3O2═2CO2+4H2O2。下列说法正确的是()。
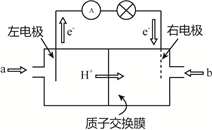
A.左电极为电池的正极,a处通入的物质是甲醇
B.右电极为电池的负极,b处通入的物质的空气
C.负极反应式为:CH3OH+H2O-6e-═CO2↑+6H+
D.正极反应式为:O2+2H2O+4e-═4OH-
(1)LiCoO2=Li1-xCoO2+xLi++xe-
(2)C+xLi++xe-=CLix
请问:(1)指出正极材料和正极反应;
(2)指出负极材料和负极反应;
(3)写出该电池总反应。


 如果结果不匹配,请
如果结果不匹配,请 
















