 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列叙述正确的是(用NA代表阿伏加德罗常数的值)()
A.2.4 g金属镁变为镁离子时失去的电子数为0.1NA
B.1 mol HCl气体中的粒子数与0.5 mol/L盐酸中的溶质粒子数相等
C.在标准状况下,22.4 L CH4与18 g H2O所含有的电子数均为10NA
D.O和N2为等电子体,22.4 L的CO气体与1 mol N2所含的电子数相等
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.2.4 g金属镁变为镁离子时失去的电子数为0.1NA
B.1 mol HCl气体中的粒子数与0.5 mol/L盐酸中的溶质粒子数相等
C.在标准状况下,22.4 L CH4与18 g H2O所含有的电子数均为10NA
D.O和N2为等电子体,22.4 L的CO气体与1 mol N2所含的电子数相等
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列叙述正确的是(用NA代表阿伏加德罗常数的值)()”相关的问题
更多“下列叙述正确的是(用NA代表阿伏加德罗常数的值)()”相关的问题
A.常温常压下,22.4 L CCl4、CO2含有的分子数为1NA
B.常温常压下,1.06 g Na2CO3含有的Na+离子数为0.02NA
C.通常状况下,NA个CO2分子占有的体积约为22.4 L
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为1NA
A.1 mol甲基(—CH3)所含的电子数为10NA
B.常温常压下,1 mol分子式为C2H6O的有机物中,含有C—O键的数目为NA
C.14 g由乙烯和环丙烷()组成的混合气体中,含有的原子总数为3NA
D.标准状况下,22.4 L四氯化碳中含有共用电子对的数目为4NA
A.常温下,pH=1的盐酸中含有H+的数目为0.1NA
B.标准状况下,22.4 L Cl2与Fe完全反应时,转移电子数为3NA
C.32 g O2和32 g O3中所含原子数均为2NA
D.常温常压下,28 g乙烯含有2NA个碳碳双键
A.水的摩尔质量为18g
B.1 mol/L K2SO4溶液所含K+数目为2NA
C.在常温常压下,2g氢气的体积为22.4L
D.1 mol Mg2+的质量为24g
用NA代表阿伏加德罗常数的值,下列说法正确的是()。
A.
所含共价键数目均为0.4NA的白磷(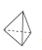 )和甲烷的物质的量相等
)和甲烷的物质的量相等
B.1molNa2O2与足量CO2充分反应转移的电子数目为2N
C.25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH﹣数目为0.2NA
D.常温下,向1L0.1mol•L﹣1醋酸钠溶液中加入醋酸至中性,则溶液中CH3COO﹣的数目为0.1NA
A.30gC2H6中含有的共价键数为6NA
B.1molN2与4molH2反应生成的NH3分子数为2NA
C.28gC2H4和CO的混合气体中含有的分子数为NA
D.2L0.5mol•L-1醋酸溶液中含有的H+数为NA
A.1L 0.1 mol/L CH3COOH中含有CH3COO-数为0.1NA
B.12g C-14所含原子数为NA
C.23gNa与氧气完全反应生成Na2O,转移的电子数为2NA
D.常温常压下,4.4g由CO2气体中含有的原子总数为0.3NA
A.常温常压下,64gSO2中含有的原子数为3NA
B.标准状况下,11.2LCCl4所含原子数目为2.5NA
C.2L0.1mol•L﹣1K2SO4溶液中含K+物质的量为0.2mol
D.1.0molCH4与Cl2在光照下反应生成的CH3Cl分子数为1.0NA
A.1 mol·L-1盐酸中,Cl-数为NA
B.58 g正丁烷中,共价键数为10 NA
C.常温常压下,2. 24 L O2中氧分子数为0.2NA
D.密闭容器中,3 mol H2和1 mol N2充分反应后原子数为8NA
A.常温常压下,4.4gCO2气体中含有的质子数为2.2NA
B.0.1molNa2O2与水充分反应转移的电子数目为0.2NA
C.1mol熔融NaHSO4电离出的阴、阳离子总数目为3NA
D.1mol甲酸中含有共用电子对的数目为4NA
A.78gNa2 O2中含有的离子总数为4NA
B.任何条件下0.5mol氨气的分子数一定是0.5NA
C.71g氯气与足量铁粉充分反应,转移的电子数为3NA
D.1L 1mol⋅L-1的盐酸中所含粒子总数为2N A