 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
有效地址EA的计算方法为()。
A.EA=基址+(变址-比例因子)+位移量
B.EA=基址+(变址×比例因子)+位移量
C.EA=基址+(变址+比例因子)+位移量
D.EA=基址+(变址×比例因子)-位移量
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.EA=基址+(变址-比例因子)+位移量
B.EA=基址+(变址×比例因子)+位移量
C.EA=基址+(变址+比例因子)+位移量
D.EA=基址+(变址×比例因子)-位移量
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“有效地址EA的计算方法为()。”相关的问题
更多“有效地址EA的计算方法为()。”相关的问题
A.指数形式为k=Aexp(-Ea/RT)
B.一般温度范围内Ea及A均不随温度变化而变化
C.常用对数形式为lgk=Ea/2.303RT=lgA
D.自然对数形式为lnk=lnA-Ea/RT
A.负电荷,Ea>Eb
B.负电荷,Ea<Eb
C.正电荷,Ea>Eb
D.正电荷,Ea<Eb
已知反应2H2O2====2H2O+O2的活化能Ea为71kJ·mol-1,在过氧化氢酶的催化下,活化能降至8.4kJ·mol-1。试计算298K时在酶催化下,H2O2分解速率为原来的多少倍?
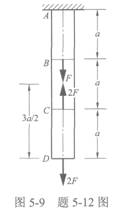
如图5-9所示等直杆,杆长为3a,材料的拉压刚度为EA,受力如图示。问杆中点横截面的铅垂位移为()。

某药物A的分解反应为一级反应,测得A在60℃分解的半衰期为0.21h,在30℃的半衰期为7.13h。计算此反应的活化能Ea和药物A保存在10℃时的半衰期。
碘化氢的分解反应为均相二级反应 2HI(g)=H2(g)+I2(g) 已知反应的活化能Ea为185kJ.mol-1,分子的碰撞直径为3.50×10-10m。试确定反应速率常数kHI与温度的关系式并求556K时的反应速率常数。