 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
(1)根据电极点位表数据计算反应:的平衡常数K.(2)现将空气(=20.3kPa)通入到含有0.10mol·dm
(1)根据电极点位表数据计算反应:
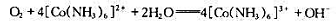
的平衡常数K.
(2)现将空气(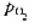 =20.3kPa)通入到含有0.10mol·dm-3[Co(NH3)6]3+,0.10mol·dm-3
=20.3kPa)通入到含有0.10mol·dm-3[Co(NH3)6]3+,0.10mol·dm-3
[Co(NH3)6]3+,2.0mol·dm-3NH2+及2.0mol·dm-3NH3·H2O的混合溶液中,能否发生上述反应?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
(1)根据电极点位表数据计算反应:
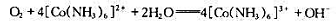
的平衡常数K.
(2)现将空气(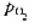 =20.3kPa)通入到含有0.10mol·dm-3[Co(NH3)6]3+,0.10mol·dm-3
=20.3kPa)通入到含有0.10mol·dm-3[Co(NH3)6]3+,0.10mol·dm-3
[Co(NH3)6]3+,2.0mol·dm-3NH2+及2.0mol·dm-3NH3·H2O的混合溶液中,能否发生上述反应?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“(1)根据电极点位表数据计算反应:的平衡常数K.(2)现将空…”相关的问题
更多“(1)根据电极点位表数据计算反应:的平衡常数K.(2)现将空…”相关的问题
工业生产SO2Cl2(1)有以下两种方法:
SO2(g)+C(g)=SO2Cl2(1)①
SO2(g)+2HCl(g)=SO2Cl2(1)+H2O(1)②
(1)请根据热力学数据计算说明,欲得到更大的转化率,应采用什么路线更好?
(2)对于②反应,增大体系温度,对反应有什么影响?
(3)求反应①在298K时的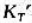
研究下面的系统函数:
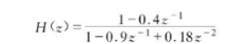
(a)计算H(z)的零点和极点。
(b)若系数舍入成4位(包括符号位)的定点补码表示,计算系统函数系数量化后的零点和极点。
1073K时,在密闭容器中进行如下可逆反应:

反应的标准平衡常数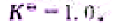
(1)如果反应开始时CO和H2O的分压都是100kPa,计算CO的平衡转化率;
(2)如果反应开始时CO的分压为100kPa,H2O的分压为500kPa,计算CO的平衡转化率。
用CaO(s)吸收高炉废气中的SO3气体,其反应方程式为
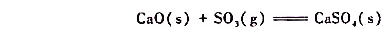
根据下列热力学数据计算该反应373K时的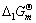 ,以说明反应进行的可能性;并计算反应逆转的温度,进一步说明应用此反应防止S03污染环境的合理性。
,以说明反应进行的可能性;并计算反应逆转的温度,进一步说明应用此反应防止S03污染环境的合理性。

如图所示,无摩擦、无质量、无体积的活塞1,2,3将反应器隔成甲、乙、丙3部分,分别进行反应
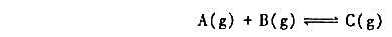
起始时物质的量已标在图中。某温度和100kPa下实现平衡时,各部分的体积分别为V甲,V乙,V丙。
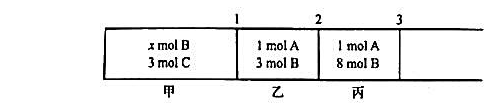
(1)这时若去掉活塞1,不会引起其他活塞移动,求算x值;
(2)去掉活塞2后再次达到平衡时,活塞3向哪个方向发生了移动?试通
过计算加以解释,可以假定反应的Kθ等于1。
表中为某企业近年来的总成本和产量的数据:
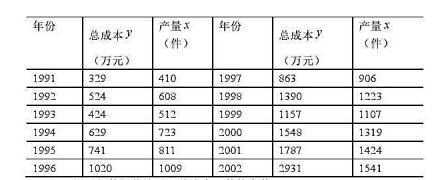
(1)用已知数据估计以下总成本函数的参数:
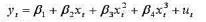
(2)检验参数的显著性;
(3)检验整个回归方程的显著性;
(4)计算总成本对产量的非线性相关指数;
(5)评价此回归分析存在什么不足。
有人对反应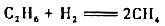 提出如下机理:
提出如下机理:
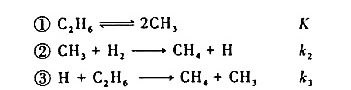
试用稳态近似法和平衡假设法推导生成CH4的速率方程微分表达式,并用已知数据K,k2,k3表示速率常数k。
将电对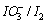 和
和 电对的电势-pH图画在同一直角坐标系中。指出体系中涉及的歧化反应和逆歧化反应发生的具体pH范围。若在298K,pH=11时将所发生的反应以原电池方式完成,试计算原电池的电动势E和电池反应的
电对的电势-pH图画在同一直角坐标系中。指出体系中涉及的歧化反应和逆歧化反应发生的具体pH范围。若在298K,pH=11时将所发生的反应以原电池方式完成,试计算原电池的电动势E和电池反应的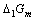 。
。
298K时,在Fe3+,Fe2+的混合溶液中加入NaOH时,有Fe(OH)3和Fe(OH)2沉淀生成(假如没有其它反应发生)。当沉淀反应达到平衡时,保持c(OH-)=1.0molL-1,计算
