 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列哪个方法一般情况下不用来计算焓变()
A.某一反应的逆反应焓变等于正反应焓变的相反数
B.通过焓的定义计算(H=U+PV)
C.通过物质的标准摩尔生成焓计算
D.赫兹定律
 答案
答案
B、通过焓的定义计算(H=U+PV)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.某一反应的逆反应焓变等于正反应焓变的相反数
B.通过焓的定义计算(H=U+PV)
C.通过物质的标准摩尔生成焓计算
D.赫兹定律
 答案
答案
B、通过焓的定义计算(H=U+PV)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列哪个方法一般情况下不用来计算焓变()”相关的问题
更多“下列哪个方法一般情况下不用来计算焓变()”相关的问题
根据下列反应在298.15K时的焓变值,计算AgCl(s)的标准摩尔生成焓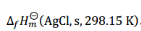
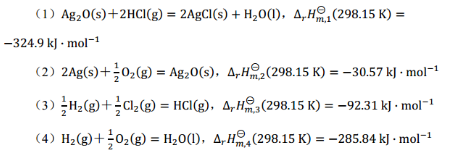
已知下列反应的标准摩尔焓变,计算298K时SiC(s)的ΔH。
(1) C(s)+O2(g)====CO2(g),ΔH=-393.5 kJ·mol-
(2) Si(s)+CO2(g)====Si(s)+O2(g),△H=-989.2kJ/mol
A.室内散发余热。余湿较多时
B.空调区换气次数较高时
C.夏季空调系统的回风比焓高于室外空气比焓时
D.空调区排风量大于按负荷计算的送风量时
在用硝石制硝酸时,下列反应同时发生: (1)KNO3(S)+H2SO4(l)=KHSO4(S)+HNO3(g) (2)2KNO3(S)+H2SO4(l)=K2SO4(S)+2HNO3(g) 制得的硝酸80%是由反应(1)产生的,20%是由反应(2)产生的。 问在25℃制取1kg HNO3(g)时将放出多少热量? 已知KNO3、H2SO4、KHSO4、HNO3、K2SO4的标准摩尔生成焓依次为-494.63、813.99、-1 160.6、135.6、-1 437.79(单位:KJmol-1) 首先必须计算上述反应的标准摩尔焓变,然后才能计算制取1kg HNO3(g)时将放出多少热量。
反应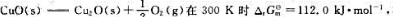 在400K时
在400K时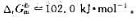
(1)计算上述反应在298.15K时的标准摩尔焓变和标准摩尔熵变;
(2)在标准状态下,该反应自发进行的最低温度是多少?
计算合成氨反应N2(g)+3H2(g)=2NH3(g)在673K时的标准平衡常数,并指出在673K,下列三种情况下反应向何方向进行? (1)P(NH3)=304kPa,P(N2)=171 kPa,P(H2)=2 022kPa; (2)p(NH3)=600kPa,P(N2)=625kPa,P(H2)=1 875kPa; (3)p(NH3)=100kPa,P(N2)=725kPa,P(H2)=2 175kPa。 在没有平衡浓度或平衡分压时,标准平衡常数KΘ 可由标准吉布斯函数变[△rGΘm]求得:△rGΘm(T)=-RTlnKΘ ,而 △rGΘm(T)≈△rHΘm(298K)-T△rSΘm(298K),所以,可根据热力学数据表中反应物和生成物的标准摩尔生成焓△rHΘm(298K)和标准摩 尔熵SΘm(298K)计算反应的标准焓变△rHΘm(298K)和标准熵变 △rSΘm(298K),进而计算出标准平衡常数KΘ。 气体反应在一定反应物和生成物分压下的方向,可由反应商J与平衡常数KΘ相对大小进行判断。
298.15K时,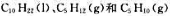 的标准摩尔燃烧焓分别为-6752kJ·mol- 1、-3492kJ·mol-1和-3364kJ·mol-1。计算298.15K裂解反应
的标准摩尔燃烧焓分别为-6752kJ·mol- 1、-3492kJ·mol-1和-3364kJ·mol-1。计算298.15K裂解反应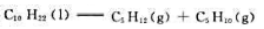 的标准摩尔焓变。
的标准摩尔焓变。
试查阅附录3的数据计算下列反应的△rHΘm(298.15 K)。 (1)4NH3(g)+3O2(g) 2N2(g)+6H2O(1) (2)C2H2(g)+H2(g)=C2H4(g) (3)NH3(g)+稀盐酸 (4)Fe(s)+CuSO4(aq) 分析本题主要考查利用标准热力学数值ArHΘm求反应焓变△rHΘm查△fHΘm数据时要注意物质的状态,对于水溶液中的反应可抓住其实质——离子反应进行计算。