 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
称取纯Fe2O3和Al2O3混合物0.5622g,在加热条件下通氢气使Fe2O3还原为F
e,冷却后称其质量为0.4582g。分别计算Fe和Al的质量分数。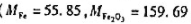
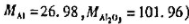
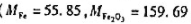
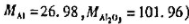
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
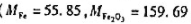
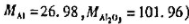
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“称取纯Fe2O3和Al2O3混合物0.5622g,在加热条件…”相关的问题
更多“称取纯Fe2O3和Al2O3混合物0.5622g,在加热条件…”相关的问题
称取铁样0.2801g,溶解后,将溶液中的Fe3+还原为Fe2+,然后用0.02000mol·L-1
K2Cr2O7标准溶液滴定,用去25.60mL,试计算:(1)K2Cr2O7标准溶液对Fe及(Fe2O3)滴定度;(2)试样中w(Fe)和w(Fe2O3).
称取含惰性杂质的混合碱(Na2CO3和NaOH或NaHCO3和Na2CO3的混合物)试样1.00g。溶于水后,用酚酞作指承剂,用0.2500mol·L-1HCl滴至终点,消耗HCl 20.40mL然后加入甲基橙指示剂,用HCl继续滴至橙色出现,又用去28.46mL试判断试样由何种碱组成?各组分的质量分数是多少?已知M(Na2CO3)=106.00g·mol-1;M(NaHCO3)=84.01g·mol-1。
配制100ml1mg/ml氨标准储备液时,需称取()经105℃干燥的分析纯氯化铵
A0.3142g2h
B0.3142g1h
C0.3412g2h
D0.3412g1h
(1)实际上所配缓冲溶液的pH为多少?
(2)若要配制pH=0.64三氯乙酸缓冲溶液。需加入多少摩尔强酸或强碱?
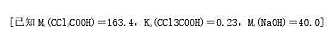
重量法测Fe,试样质量0.1666g,沉淀Fe2O3称重为0.1370g,求w(Fe),w(Fe3O4)?
A.0.1~0.2
B.0.2~0.3
C.0.3~0.4
D.0.5~0.6
己知某一混合物中包含N个组分,且其包含的各个组分的纯物质谱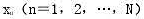 已知,若测得该系列混合物在L个分析通道处获得的分析信号为Y,设分析信号
已知,若测得该系列混合物在L个分析通道处获得的分析信号为Y,设分析信号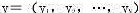 与样本中各组分的浓度
与样本中各组分的浓度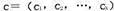 服从以下关系:
服从以下关系:
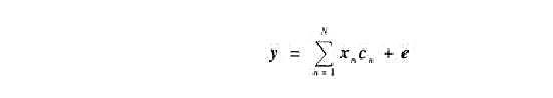
试估计该混合物中各组分的浓度(写出计算式)。