 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
将30 mL0.5mol/LNaOH溶液加水稀释到500 mL,稀释后溶液中NaOH的物质的量浓度为()
A.0.3mol/L
B.0.03mol/L
C.0.005mol/L
D.0.04mol/L
 答案
答案
B、0.03mol/L
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.0.3mol/L
B.0.03mol/L
C.0.005mol/L
D.0.04mol/L
 答案
答案
B、0.03mol/L
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“将30 mL0.5mol/LNaOH溶液加水稀释到500 m…”相关的问题
更多“将30 mL0.5mol/LNaOH溶液加水稀释到500 m…”相关的问题
用NaAc?3H2O晶体,2.0mol/LNaOH来配制PH为5.0的HAc-NaAc缓冲溶液1升,其正确的配制是()。
A.将49克NaAc?3H2O放入少量水中溶解,再加入50ml2.0mol/LHAc溶液,用水稀释1升
B.将98克NaAc?3H2O放入少量水中溶解,再加入50ml2.0mol/LHAc溶液,用水稀释1升
C.将25克NaAc?3H2O放入少量水中溶解,再加入100ml2.0mol/LHAc溶液,用水稀释1升
D.将49克NaAc?3H2O放入少量水中溶解,再加入100ml2.0mol/LHAc溶液,用水稀释1升
用邻苯二甲酸氢钾为基准物标定0.1mol/LNaOH溶液,每份基准物的称取量宜为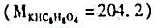 ()。
()。
A.0.2g
B.0.2~0.4g
C.0.4~0.5g
D.>0.5g
准确量取30.00ml弱酸,加水稀释至100ml。以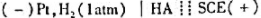 为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
(1)弱酸HA的Ka。
(2)原弱酸HA的浓度。
A.HAc(Ka=1.75×10-5)
B.次溴酸(Ka=2.30×10-9)
C.HCN(Ka=6.20×10-10)
D.丙二酸(Ka1=1.42×10-3,Ka2=2.01×10-6)