 更多“配制100ml的0.1mol/LNaOH溶液的主要步骤有计算…”相关的问题
更多“配制100ml的0.1mol/LNaOH溶液的主要步骤有计算…”相关的问题
第1题
若要配制0.1mol/LCuSO4溶液100ml,需CuSO4晶体()克(已知CuSO4·5H2O的摩尔质量为250g/mol)。
若要配制0.1mol/LCuSO4溶液100ml,需CuSO4晶体()克(已知CuSO4·5H2O的摩尔质量为250g/mol)。
第2题
用邻苯二甲酸氢钾为基准物标定0.1mol/LNaOH溶液,每份基准物的称取量宜为( )。
用邻苯二甲酸氢钾为基准物标定0.1mol/LNaOH溶液,每份基准物的称取量宜为()。
点击查看答案
用邻苯二甲酸氢钾为基准物标定0.1mol/LNaOH溶液,每份基准物的称取量宜为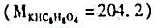 ()。
()。
A.0.2g
B.0.2~0.4g
C.0.4~0.5g
D.>0.5g
第3题
准确量取30.00ml弱酸,加水稀释至100ml。以为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被
准确量取30.00ml弱酸,加水稀释至100ml。以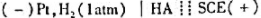 为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
(1)弱酸HA的Ka。
(2)原弱酸HA的浓度。
第6题
配制高锰酸钾溶液c(KMnO4)=0.1mol/L,则高锰酸钾基本单元的浓度[c(1/5KMnO4)]是()。
A.0.02mo1/L
B.0.1mol/L
C.0.5mol/L
D.0.25mo1/L
第7题
用NaAc?3H2O晶体,2.0mol/LNaOH来配制PH为5.0的HAc-NaAc缓冲溶液1升,其正确的配制是()。
A.将49克NaAc?3H2O放入少量水中溶解,再加入50ml2.0mol/LHAc溶液,用水稀释1升
B.将98克NaAc?3H2O放入少量水中溶解,再加入50ml2.0mol/LHAc溶液,用水稀释1升
C.将25克NaAc?3H2O放入少量水中溶解,再加入100ml2.0mol/LHAc溶液,用水稀释1升
D.将49克NaAc?3H2O放入少量水中溶解,再加入100ml2.0mol/LHAc溶液,用水稀释1升
第9题
用37%的浓盐酸(密度为1.18g£¯mL)配制0.1mol£¯L的盐酸溶液1000mL,需要移取浓盐酸()。
A.5.64mL
B.8.33mL
C.10.22mL
D.16.6mL
第10题
取水样100ml监测其COD,按标准方法将水样和空白样加热回流,滴定时水样消耗浓度为0.1mol/L的硫酸亚铁铵30ml,空白样消耗48.5ml,试计算此水样中COD的含量。(以O,mg/L表示)(M1/2O=8)。
第11题
配制0.5升0.1mol/L Na2CO3溶液:在天平上称量()克无水Na2CO3放入()中,用适量蒸馏水使其完全溶解
配制0.5升0.1mol/L Na2CO3溶液:在天平上称量()克无水Na2CO3放入()中,用适量蒸馏水使其完全溶解。

 如果结果不匹配,请
如果结果不匹配,请 
















