 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
写出下列物质间反应的化学方程式()
A.(1)2-溴丙烷消去反应
B.(2)实验室制乙烯
C.(3)苯酚与浓溴水
D.(4)乙二醇催化氧化
E.(5)苯甲醛与氢气
 答案
答案
(1)2-溴丙烷消去反应
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.(1)2-溴丙烷消去反应
B.(2)实验室制乙烯
C.(3)苯酚与浓溴水
D.(4)乙二醇催化氧化
E.(5)苯甲醛与氢气
 答案
答案
(1)2-溴丙烷消去反应
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“写出下列物质间反应的化学方程式()”相关的问题
更多“写出下列物质间反应的化学方程式()”相关的问题
工业上用铝土矿(主要成分为氧化铝,含少量氧化铁)制取铝的过程如图所示: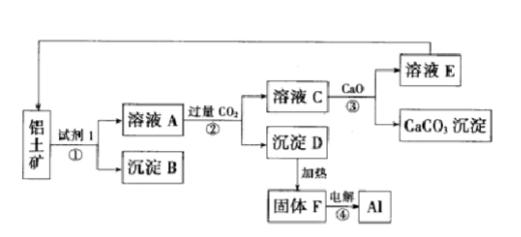 请回答:
请回答:
(1)试剂Ι为()(填化学式),①-④转化中属于氧化还原反应的是()(填序号);
(2)沉淀B的化学式为(),写出该物质发生铝热反应的化学方程式();
(3)电解F,当转移0.6mol,电子时,可制得铝()g;
(4)沉淀D是药物“胃舒平”的主要成分,可用于治疗胃酸(稀盐酸)过多,写出该反应的离子方程式();
(5)②中发生反应的离子方程式为()。
某校化学研究性学习小组的同学在学习了氨的性质后讨论:运用类比的思想,既然氨气具有还原性,能否像H2那样还原Cu0呢?他们设计实验制取氮气并探究上述问题。请你参与该小组的活动并完成下列研究:
(一)制取氨气
(1)写出实验制取氨气的化学方程式()。
(2有同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气。你认为他能否达到目的()(填“能”或“否”)。理由是()。
(二)该小组中某同学设计了下图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性: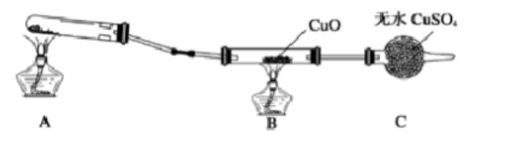 ⑴该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是:()。
⑴该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是:()。
(2)利用改进后的装置进行实验,观察到Cu0变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体。写出氨气与Cu0反应的化学方程式()。
(三)问题讨论:
有同学认为:NH3与Cu0反应生成的红色物质中可能含有Cu20.已知:Cu20是一种碱性氧化物;在酸性溶液中,Cu'的稳定性差(Cu+→Cu+Cu2+)。请你设计一个简单的实验检验该红色物质中是否含有Cu0:()。
如图所示中,A是一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应的火焰均呈黄色。
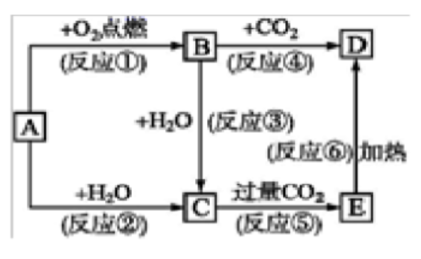 填写下列空白:
填写下列空白:
(1)写出化学式:A(),B(),D()。
(2)以上反应中属于氧化还原反应的有()(填序号)。
(3)写出反应⑤的离子方程式:()。
写出反应⑥的化学方程式:()。
铋及其化合物在工业生产中用途广泛,某研究小组用浮选过的辉铋矿(主要成分是Bi2S3,还含少量SiO2等杂质)制备NaBiO3,其流程如下: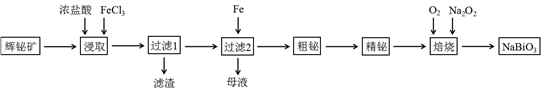 已知:①铋酸钠是一种难溶于水的物质;②水解能力:Bi3+>Fe3+。
已知:①铋酸钠是一种难溶于水的物质;②水解能力:Bi3+>Fe3+。
回答下列问题:
(1)“浸取”时,为了提高浸取速率,可采取的措施有()(任写一条);过滤1的滤渣中的某种主要成分可溶于一种弱酸,写出该反应的化学方程式()。
(2)浸取时加入过量浓盐酸的目的是()。
(3)写出焙烧时生成铋酸钠的化学方程式()。
(4)用H2Dz(双硫腙,二元弱酸)~CCl4络合萃取法可从工业废水中提取金属离子:H2Dz先将金属离子络合成电中性的物质[如Cu(HDz)2等],再用CCl4萃取此络合物。下图是用上述方法处理含有Hg2+、Bi3+、Zn2+的废水时的酸度曲线(E%表示金属离子以络合物形式被萃取分离的百分率)。
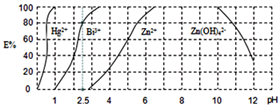 ①当n(Bi3+):n[Bi(HDz)3]=1:4时,废水的pH=()。
①当n(Bi3+):n[Bi(HDz)3]=1:4时,废水的pH=()。
②向萃取后的CCl4中加入足量的NaOH溶液可将Bi(HDz)3中铋元素以氢氧化物的形式沉淀下来,相应的离子方程式为()。
(5)取焙烧得到的NaBiO3样品加入稀硫酸和MnSO4溶液使其完全溶解。已知NaBiO3被还原为Bi3+,Mn2+被氧化成MnO4-,试写出该反应的离子方程式:()。
以黄铜矿为主要原料来生产铜、铁红颜料和硫单质,原料的综合利用率较高。其主要流程如下: 问题一、过滤③得到的滤渣成分是:()。(填化学式)
问题一、过滤③得到的滤渣成分是:()。(填化学式)
问题二、反应Ⅰ~Ⅴ中,共有()个反应不属于氧化复原反应。
问题三、溶液A中含有的溶质是()。(填化学式)
问题四、写出反应Ⅰ的化学方程式:()。
问题五、反应Ⅲ是是FeCO3在空气中煅烧,写出化学方程式:()。
A.必须遵循质量守恒定律
B.一定要注明反应条件
C.不用注明生成物的颜色
D.在方程式配平的过程中,可以改动物质的化学式,这样可以使配平容易些