 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
测定硫酸铜晶体中结晶水含量实验,经计算相对误差为+0.4%,则下列对实验过程的相关判断合理的为()
A.所用晶体中含有硫酸钡
B.所用晶体中外表面含有游离态的水
C.加热后的坩埚放在干燥器中冷却
D.没有进行恒重操作
 答案
答案
B、所用晶体中外表面含有游离态的水
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.所用晶体中含有硫酸钡
B.所用晶体中外表面含有游离态的水
C.加热后的坩埚放在干燥器中冷却
D.没有进行恒重操作
 答案
答案
B、所用晶体中外表面含有游离态的水
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“测定硫酸铜晶体中结晶水含量实验,经计算相对误差为+0.4%,…”相关的问题
更多“测定硫酸铜晶体中结晶水含量实验,经计算相对误差为+0.4%,…”相关的问题
A.①②
B.①③
C.①③⑤
D.②④⑤
A.配制5%食盐溶液时,将称量的食盐放入烧杯中加计量的水搅拌溶解
B.铜结晶水含量测定时,需用小火缓慢加热,防止晶体飞溅
C.测定未知NaOH溶液浓度时,酸式滴定管需用标准酸液润洗2—3次
D.配制0.1mol/L的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释
A.滴定管洗净后经蒸馏水润洗,即可注入标准液进行滴定
B.玻璃导管蘸水后,边旋转边向橡皮管中插入
C.加热热坩埚中的硫酸铜晶体,失水后须在干燥器中冷却,再称量
D.玻璃棒蘸取溶液滴到放在表面皿上的pH试纸上
A.用加热法测定硫酸铜晶体里的结晶水数目
B.用99%的乙醇稀释成75%(体积分数)的医用酒精
C.用98% 的浓硫酸配制500g质量分数为10%的稀硫酸
D.滴入适量的氯化钡溶液将3mL某溶液里的硫酸根离子沉淀完全
用加热法驱除水分以测定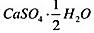 中结晶水的含量.称取试样0.2000g,已知天平称量误差为±0.1mg,试问分析结果应以几位有效数字报出?
中结晶水的含量.称取试样0.2000g,已知天平称量误差为±0.1mg,试问分析结果应以几位有效数字报出?
某废催化剂主要成分有SiO2、ZnO、ZnS和CuS。某化学兴趣小组拟用该废催化剂为原料,制备硫酸锌和硫酸铜晶体。采用的实验方案如下,下列说法正确的是()。 已知:ZnS与稀硫酸发生反应且化合价不变,CuS既不溶于稀硫酸也不和稀硫酸反应
A.第一次浸出可以在烧杯中进行
B.第二次浸出时发生反应为CuS+H2O2+H2SO4=CuSO4+S+2H2O
C.滤渣2中只有二氧化硅
D.获得硫酸锌和硫酸铜晶体采用蒸发结晶的方式
A.①中溶液的溶质质量分数为16%
B.②中加入氢氧化钠的过程中,有氢氧化钙析出
C.③中棉线上析出晶体的质量一定是34.3g
D.④中加入氢氧化钠前、后均为硫酸铜饱和溶液
A.吸取氢氧化钠溶液后的胶头滴管可直接再吸取氢氧化钙溶液
B.为减少实验误差,在量筒内溶解氯化钠
C.为防止产生的液体洒落,加热硫酸铜晶体时将试管口略向上倾斜
D.做蜡烛在氧气中燃烧的实验时用向上排空气法收集所需的氧气