 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
计算浓度为0.12mol·L-1的下列物质水溶液的pH(括号内为pKa).(1)苯酚(9.95);(2)丙烯酸(4.25);(3)吡啶的硝酸盐(C5H5NHNO3)(5.23).
计算浓度为0.12mol·L-1的下列物质水溶液的pH(括号内为pKa).(1)苯酚(9.95);(2)丙烯酸(4.25);(3)吡啶的硝酸盐(C5H5NHNO3)(5.23).
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“计算浓度为0.12mol·L-1的下列物质水溶液的pH(括号…”相关的问题
更多“计算浓度为0.12mol·L-1的下列物质水溶液的pH(括号…”相关的问题
应速率为0.10mol·L-1s-1,计算:(1)速率常数k;(2)当c(H2)=0.60mol·L-1,c(I2)=0.1mol·L-1,c(HI)=0.20mol·L-1时的起始反应速率.
蔗糖水解反应为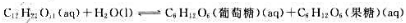 当蔗糖的起始浓度为amol·L-1时,在温度T时水解反应达到平衡时蔗糖水解了1/3,试计算该温度下蔗糖水解反应的标准平衡常数。
当蔗糖的起始浓度为amol·L-1时,在温度T时水解反应达到平衡时蔗糖水解了1/3,试计算该温度下蔗糖水解反应的标准平衡常数。
(1)每升碱液吸收了多少克CO2?
(2)用该碱液滴定某一元弱酸,若浓度仍以0.1026ml·L-1计算,会引起多大误差?
0.29molNH3溶解在0.45L0.36mol·L-1的AgNO3溶液中,已知:
NH3K(NH4·H4O)=1.8X10-5,K[Ag(NH3)2]+=1.1X107,计算平衡时各种物质的浓度.
A.1.0×10-4mol·L-1
B.1.0×10-7mol·L-1
C.0.10mol·L-1
D.1.0X10-12mol·L-1
A.0.51
B.0.45
C.0.15
D.0.13
度为1.0×10mol·L-5,铁电对的电势是多少?共存的Fe(Ⅲ) 对测定有无干扰?若加入EDTA并使其过量的浓度为0.10mol·L-1,问此条件下, 铁电对的条件电势是多少?Fe(III) 的干扰能否被消除?