 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
100kPa下,冰(H2O,s)的熔点为0°C在此条件下冰的摩尔融化热已知在-10°C~0°C范围内过冷水(H≇
100kPa下,冰(H2O,s)的熔点为0°C在此条件下冰的摩尔融化热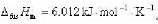 已知在-10°C~0°C范围内过冷水(H2O,l)和冰的摩尔定压热容分别为Cp,m(H2O,l)=76.281mol-1·K-1和Cp,m(H2O,s)=37201mol-1·K-1.求在常压及10°C下过冷水结冰的摩尔凝固焓。
已知在-10°C~0°C范围内过冷水(H2O,l)和冰的摩尔定压热容分别为Cp,m(H2O,l)=76.281mol-1·K-1和Cp,m(H2O,s)=37201mol-1·K-1.求在常压及10°C下过冷水结冰的摩尔凝固焓。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
100kPa下,冰(H2O,s)的熔点为0°C在此条件下冰的摩尔融化热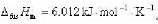 已知在-10°C~0°C范围内过冷水(H2O,l)和冰的摩尔定压热容分别为Cp,m(H2O,l)=76.281mol-1·K-1和Cp,m(H2O,s)=37201mol-1·K-1.求在常压及10°C下过冷水结冰的摩尔凝固焓。
已知在-10°C~0°C范围内过冷水(H2O,l)和冰的摩尔定压热容分别为Cp,m(H2O,l)=76.281mol-1·K-1和Cp,m(H2O,s)=37201mol-1·K-1.求在常压及10°C下过冷水结冰的摩尔凝固焓。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“100kPa下,冰(H2O,s)的熔点为0°C在此条件下冰的…”相关的问题
更多“100kPa下,冰(H2O,s)的熔点为0°C在此条件下冰的…”相关的问题
1073K时,在密闭容器中进行如下可逆反应:

反应的标准平衡常数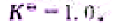
(1)如果反应开始时CO和H2O的分压都是100kPa,计算CO的平衡转化率;
(2)如果反应开始时CO的分压为100kPa,H2O的分压为500kPa,计算CO的平衡转化率。
A.6x10-3;
B.6;
C.6000;
D.0.6
1373K时,可逆反应 若在一密闭容器中CO和H2O的分压都为200kPa,CO2和H2的分压都为100kPa时,它们的分压是否发生变化?计算出达到化学平衡后各气体的分压。
若在一密闭容器中CO和H2O的分压都为200kPa,CO2和H2的分压都为100kPa时,它们的分压是否发生变化?计算出达到化学平衡后各气体的分压。
在600℃,100kPa时下列反应达到平衡:
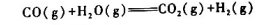
现在把压力提高到5×104kPa,问:
(1)若各气体均视为理想气体,平衡是否移动?
(2)若各气体的逸度因子分别为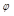 (CO2)=1.09,
(CO2)=1.09,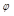 (H2)=1.10,
(H2)=1.10,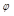 (CO)=1.20,
(CO)=1.20,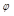 (H2O)=0.75,与理想气体反应相比,平衡向哪个方向移动?
(H2O)=0.75,与理想气体反应相比,平衡向哪个方向移动?
在常温真实溶液中,溶质B的化学势可表示为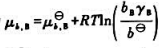 ,式中B的标准态为温度T、压力p=pθ=100kPa下,
,式中B的标准态为温度T、压力p=pθ=100kPa下,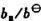 =(),
=(),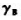 =(),同时又遵循亨利定律的假想态.
=(),同时又遵循亨利定律的假想态.
下述3个反应:①S(s)+O2(g)→SO2(g)
②H2(g)+O2(g)→H2O2(l)
③C(s)+H2O(g)→CO(g)+H2(g)
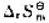 由小到大的顺序为()。
由小到大的顺序为()。
下列化学反应,同时共存并达到平衡(温度在900~1200K范围内):
CaCO3(s)=CaO(s)+CO2(g)
CO2(g)+H2(g)=CO(g)+H2O(g)
H2O(g)+CO(g) +CaO(s)=CaCO3(s)+H2(g)
问该体系的自由度数为______ 。
100kPa,25℃时,化学反应C(s)+CO2(g)→2CO(g)的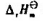 =172.46kJ,反应的
=172.46kJ,反应的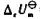 =()kJ.(设气体均可视为理想气体.)
=()kJ.(设气体均可视为理想气体.)
A.174.94;
B.169.98;
C.172.46;
D.167.50