 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
298K时,测得如下电池 Pt|H2()|HBr(m)|AgBr(s)|Ag(s) 申池的电动势E与HBr浓度的关系如表所示: m
298K时,测得如下电池
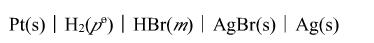
申池的电动势E与HBr浓度的关系如表所示:
| m/(mol·kg-1) | 0.01 | 0.02 | 0.05 | 0.10 |
| E/N | 0.3127 | 0.2786 | 0.2340 | 0.2005 |
试计算:

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
298K时,测得如下电池
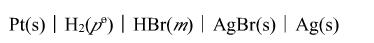
申池的电动势E与HBr浓度的关系如表所示:
| m/(mol·kg-1) | 0.01 | 0.02 | 0.05 | 0.10 |
| E/N | 0.3127 | 0.2786 | 0.2340 | 0.2005 |
试计算:

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“298K时,测得如下电池 Pt|H2()|HBr(m)|Ag…”相关的问题
更多“298K时,测得如下电池 Pt|H2()|HBr(m)|Ag…”相关的问题
298K时,测得电池Pt|H2(100kPa)|H2SO4(0.5mol/kg)|Hg2SO4(s)|Hg(l)的电动势为0.6960V,求H2SO4在溶液中的离子平均活度系数。已知 为0.6158V。
为0.6158V。
298K时,已知如下电池的标准电动势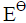 =0.2680V:
=0.2680V:
Pt|H2(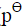 )|HCl(0.08mol·kg-1, γ±=0.809)|Hg2Cl2(s)|Hg(l)
)|HCl(0.08mol·kg-1, γ±=0.809)|Hg2Cl2(s)|Hg(l)

298K时,测得电池Pt|H2(100kPa)|H2SO4(0.5mol/kg)|Hg2SO4(s)|Hg(l)的电动势为0.6960V,求H2SO4在溶液中的离子平均活度系数。已知
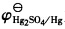 为0.6158V。
为0.6158V。
用电动势法测定丁酸的解离常数。在298K时安排成如下电池:
Pt|H2(p。)|HA(m1),NaA(m2),NaCl(m3)|AgCl(s)|Ag(s)
其中HA为丁酸,NaA为丁酸钠。实验数据如下:
| m1/(mol·kg-1) | m2/(mol·kg-1) | m3/(mol·kg-1) | E/V |
| 0.00717 | 0.00687 | 0.00706 | 0.63387 |
| 0.01273 | 0.01220 | 0.01254 | 0.61922 |
| 0.01515 | 0.01453 | 0.01493 | 0.61501 |
试求HA==H++A-的平衡常数Kθ。设活度因子均为1。
19,有电池Pt|H2(




 H+(
H+(


298K时,有电池Pt|H2(100kPa)|HI(m)|AuI(S)|Au(s)。 (1)请写出各电极反应及电池反应。 (2)m=1×10-4mol/kg时,电动势E=0.97V;若m=3.0mol/kg时,E=0.41V。求m=3.0mol/kg时,HI的平均活度系数。 (3)已知Au+(aq)+e-→Au(8)的φΘ=1.68V,求AuI的溶度积。
在298K时,下述电池的电动势E=0.1519V:
Ag(s)|AgI(s)|HI(a=1)|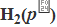 |Pt
|Pt
并已知下列物质的标准摩尔生成焓:
| 物 质 | AgI(s) | Ag+ | I- |
 | -62.38 | 105.89 | -55.94 |
试求:

根据下列在298K和标准压力下的热力学数据,计算HgO(s)在该温度时的解离压。
(1)电池Pt|H2(PH2) |NaOH(a) |HgO(s) |Hg(I)的标准电动势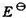 =0.9265V;
=0.9265V;
(2)反应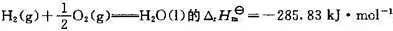 ;
;
(3)298K时,下表为各物质的标准摩尔熵值:

已知298K时,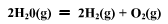 反应的平衡常数为9.7×10-81,这时H2O(1)的饱和蒸气压为3200Pa,试求298K时下述电池的电动势E。
反应的平衡常数为9.7×10-81,这时H2O(1)的饱和蒸气压为3200Pa,试求298K时下述电池的电动势E。
Pt|H2(P3)|H2SO4(0.01mol·kg-1)|O2(P3)|Pt
(298K时的平衡常数是根据高温下的数据间接求出的。由于氧电极上反应不易达到平衡,不能测出E的精确值,所以可通过此法来计算E值。)
今有原电池:
(—)Pt|H2(100kPa)|HA(0.500mol·L-1)||Cl-(1.00mol·L-1)|AgCl|Ag()
在298.15K时测得电池电动势为0.568V,试计算一元弱酸HA的酸度常数。