 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
某温度下,反应N2O4(g)≒ 2NO2(g)-Q在密闭容器中达到平衡.下列说法不正确的是()
A.加压时(体积变小),将使正反应速率增大
B.保持体积不变,加入少许NO2,将使正反应速率减小
C.保持体积不变,加入少许N2O4,再达平衡时,颜色变深
D.保持体积不变,升高温度,再达平衡时颜色变深
 答案
答案
B、保持体积不变,加入少许NO2,将使正反应速率减小
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.加压时(体积变小),将使正反应速率增大
B.保持体积不变,加入少许NO2,将使正反应速率减小
C.保持体积不变,加入少许N2O4,再达平衡时,颜色变深
D.保持体积不变,升高温度,再达平衡时颜色变深
 答案
答案
B、保持体积不变,加入少许NO2,将使正反应速率减小
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某温度下,反应N2O4(g)≒ 2NO2(g)-Q在密闭容器…”相关的问题
更多“某温度下,反应N2O4(g)≒ 2NO2(g)-Q在密闭容器…”相关的问题
A.不变
B.增大
C.减小
D.无法判断
力为1.0×10Pa时,有50%N2O4分解,试确定在N2O4起始压力为2.0×105Pa时N2O4分解的百分率,并求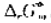 .
.
2NO2(g).25℃下该反应的初始速率实验数据如表3-1:

(1)写出反应速率方程;
(2)计算25℃时反应速度系数k;
(3)co(NO)=0.0030mol·L-2,co(O2)=0.0015rmol·L-2时,相应的初始速半为多少?
A.升高温度,反应速率减慢
B.当反应达到化学平衡时,υ(正)=υ(逆)=0
C.提高炼铁高炉的高度可减少尾气中CO的浓度
D.某温度下达到平衡时CO的体积分数基本不变
体积为1dm3的抽空密闭容器中放有0.03458molN2O4(g),发生如下分解反应:

50℃时分解反应的平衡总压为130.0kPa.已知25℃时N2O4(g)和NO2(g)的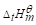
分别为9.16kJ·mol-1和33.18kJ·mol-1.设反应的ΔTGp,m=0.
(1)计算50℃时N2O4(g)的解离度及分解反应的Kθ;
(2)计算100C时反应的Kθ.
A.8.64
B.9.20
C.9.00
D.9