 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
A-B-764 4 2 3当【H+】=0.0001mol/L时,其溶液的PH值是()
A.1
B.4
C.0
D.10
 答案
答案
B、4
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.1
B.4
C.0
D.10
 答案
答案
B、4
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“A-B-764 4 2 3当【H+】=0.0001mol/L…”相关的问题
更多“A-B-764 4 2 3当【H+】=0.0001mol/L…”相关的问题
有一电池(-)Pt,H2(50kPa)|H+(0.50mol·L-1)||Sn4+(0.70mol·L-1),Sn2+(0.50mol·L-1)|Pt()
(1)写出半反应
(2)写出电池反应
(3)计算原电池的电动势E
(4)当E=0时,在保持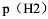 和
和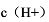 不变的情况下,
不变的情况下,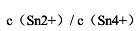 等于多少?
等于多少?
已知Eθ(MnO-4/Mn2+)=1.51V,Eθ(Cl2/Cl-)=1.36V,若将此两电对组成原电池,请写出:
(1)该电池的电池符号;
(2)写出正负电极的电极反应和电池反应以及电池标准电动势;
(3)计算电池反应在25℃时和Kθ;
(4)当[H+] = 1.0×10-2mol•L-1,而其他离子浓度均为1.0 mol•L-1,= 100 kPa时的电池电动势.