 更多“ 铁的化学元素是()。”相关的问题
更多“ 铁的化学元素是()。”相关的问题
第7题
用重量法测定某铁试样0.1600g中的铁,获得0.1300gFe2O3,试样中Fe%的计算式为:()。A.〔(0.1300×2Fe/
用重量法测定某铁试样0.1600g中的铁,获得0.1300gFe2O3,试样中Fe%的计算式为:()。
A.〔(0.1300×2Fe/Fe2O3)/0.1600〕×100
B.〔(0.1300Fe/Fe2O3)/0.1600〕×100
C.〔(0.1300×Fe/1000)/0.1600〕×100
第9题
用碘量法测定铬铁矿中铬的含量时,若溶液中Fe(III) 的浓度为0.10mol·L-1, Fe(II) 的浓
用碘量法测定铬铁矿中铬的含量时,若溶液中Fe(III) 的浓度为0.10mol·L-1, Fe(II) 的浓
点击查看答案
度为1.0×10mol·L-5,铁电对的电势是多少?共存的Fe(Ⅲ) 对测定有无干扰?若加入EDTA并使其过量的浓度为0.10mol·L-1,问此条件下, 铁电对的条件电势是多少?Fe(III) 的干扰能否被消除?
第10题
将0.5080g黄铁矿(FeS2)试样分解后,得到1.561gBaSO4。若溶液中的铁沉淀为Fe(OH)3,灼
将0.5080g黄铁矿(FeS2)试样分解后,得到1.561gBaSO4。若溶液中的铁沉淀为Fe(OH)3,灼
点击查看答案
烧可得Fe2O3多少克?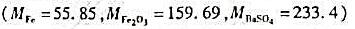
第11题
称取铁样0.2801g,溶解后,将溶液中的Fe3+还原为Fe2+,然后用0.02000mol·L-1K
称取铁样0.2801g,溶解后,将溶液中的Fe3+还原为Fe2+,然后用0.02000mol·L-1
K2Cr2O7标准溶液滴定,用去25.60mL,试计算:(1)K2Cr2O7标准溶液对Fe及(Fe2O3)滴定度;(2)试样中w(Fe)和w(Fe2O3).


 如果结果不匹配,请
如果结果不匹配,请 
















