 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
关于水的离子积常数,下列说法不正确的是()
A.蒸馏水中,c(H+)•c(OH-)=1×10-14
B.纯水中,25 ℃时,c(H+)•c(OH-)=1×10-14
C.25 ℃时,任何以水为溶剂的稀电解质溶液中,c(H+)•c(OH-)=1×10-14
D.KW值随温度升高而增大
 答案
答案
A、蒸馏水中,c(H+)•c(OH-)=1×10-14
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.蒸馏水中,c(H+)•c(OH-)=1×10-14
B.纯水中,25 ℃时,c(H+)•c(OH-)=1×10-14
C.25 ℃时,任何以水为溶剂的稀电解质溶液中,c(H+)•c(OH-)=1×10-14
D.KW值随温度升高而增大
 答案
答案
A、蒸馏水中,c(H+)•c(OH-)=1×10-14
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“关于水的离子积常数,下列说法不正确的是()”相关的问题
更多“关于水的离子积常数,下列说法不正确的是()”相关的问题
A.Na2CO3溶液中c(OH-)大于c(HCO3-)
B.Kw为水的离子积常数,若溶液中c2(OH-)=Kw,溶液pH可能小于7
C.1mol·L-1CH3COOH溶液加水稀释时,溶液中各种离子浓度均减小
D.在CH3COOH溶液中加入碱性固体物质,平衡一定向电离方向移动
A.(H+)随着温度升高而降低
B.在35℃时,c(H+)>c(OH—)
C.水的电离程度:(25℃)>(35℃)
D.水的电离是吸热的
A.此时水的离子积Kw=1×10-14
B.水电离出的c(H+)=1×10-10mol•L-1
C.水的电离程度随温度升高而增大
D.c(Na+)=c(SO42-)
已知水的离子积常数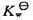 在293 K和303K时分别为
在293 K和303K时分别为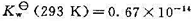 和
和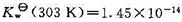 .试求:(1) 298 K和标准压力时,中和反应
.试求:(1) 298 K和标准压力时,中和反应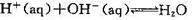 (1)的
(1)的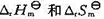 的值(设
的值(设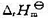 与温度的关系可以忽略);(2) 298 K时OH-的标准摩尔生成Gibbs 自由能
与温度的关系可以忽略);(2) 298 K时OH-的标准摩尔生成Gibbs 自由能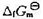 的值。
的值。
已知下述电池的标准电动势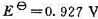 :
:
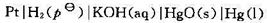
并已知反应 .
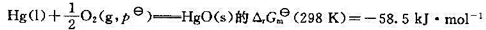
A.常温下,1LpH=10的NaClO溶液中,发生电离的水分子数为1×10-10NA
B.12gNaHSO4固体中含有的离子数为0.2NA
C.71gCl2溶于水转移的电子数为NA
D.标况下,11.2LHF含有的分子数为0.5NA
A.Mg2+:一个镁离子带2个单位正电荷
B.2H2O:水分子的个数是2个
C.H2O:水分子中含有氢原子的个数是2个
D.2H:氢原子的个数是2个
A.两种难溶强电解质相比较,标准溶度积常数较大的,其溶解度肯定也较大
B.将难溶强电解质的饱和溶液加水稀释时,难溶强电解质的标准溶度积常数不变,其溶解度也不变
C.难溶强电解质溶液的导电能力很弱,所以难溶强电解质均为弱电解质
D.难溶强电解质在水中达到溶解平衡时,电解质离子浓度的乘积就是该难溶强电解质的标准溶度积常数
A.字符串常量包括双引号本身
B.用一对双引号括起来的字符串称为字符串常量
C.数值型常量类似于数学中的常数
D.在VB中的常量有数值型常量、字符串常量等
A.分子、原子、离子都可直接构成物质
B.在化学变化中,分子可以再分,原子不能再分
C.原子得失电子后能变成离子,离子不能变成原子
D.分子由原子构成