 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
甲、乙两种固体物质(均不含结晶水)的溶解度曲线如“题12图”所示。下列说法中正确的是()
A.乙的溶解度大于甲的溶解度
B.t2℃时,乙的饱和溶液升温或降温均会析出晶体
C.甲溶液从t3℃降温到t1℃,甲溶液中溶质的质量分数会变小
D.t3℃时,50g水中加入40g的甲物质充分溶解可得到90g甲的饱和溶液
 答案
答案
B、t2℃时,乙的饱和溶液升温或降温均会析出晶体
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.乙的溶解度大于甲的溶解度
B.t2℃时,乙的饱和溶液升温或降温均会析出晶体
C.甲溶液从t3℃降温到t1℃,甲溶液中溶质的质量分数会变小
D.t3℃时,50g水中加入40g的甲物质充分溶解可得到90g甲的饱和溶液
 答案
答案
B、t2℃时,乙的饱和溶液升温或降温均会析出晶体
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“甲、乙两种固体物质(均不含结晶水)的溶解度曲线如“题12图”…”相关的问题
更多“甲、乙两种固体物质(均不含结晶水)的溶解度曲线如“题12图”…”相关的问题
A.将甲物质的溶液由t3℃降温到t2℃,一定有晶体析出
B.将甲物质的饱和溶液由t2℃升温至t3℃时,其溶质质量分数不变
C.将t3℃时三种物质的饱和溶液恒温蒸发等质量的水,析出溶质的质量:甲>乙>丙
D.将t3℃三种物质的饱和溶液降温至t2℃,所得溶液的溶质质量分数:乙>甲>丙
A.T℃时,甲、乙两物质的溶解度相等
B.乙的饱和溶液降温时,溶质质量分数保持不变
C.甲中混有少量乙,可采用降温结晶的方法提纯甲
D.T℃时,甲的饱和溶液溶质质量分数为 20%
A.M的溶解度比N大
B.t1 ℃时,接近饱和的M溶液降低温度可以达到饱和
C.t2 ℃时,100 g N的饱和溶液中溶解了30 g N物质
D.t2 ℃时,M、N溶液的溶质质量分数相等
在已知提取氯化钠、溴、镁等化学物质的富碘卤水中,采用下面的工艺流程生产单质碘: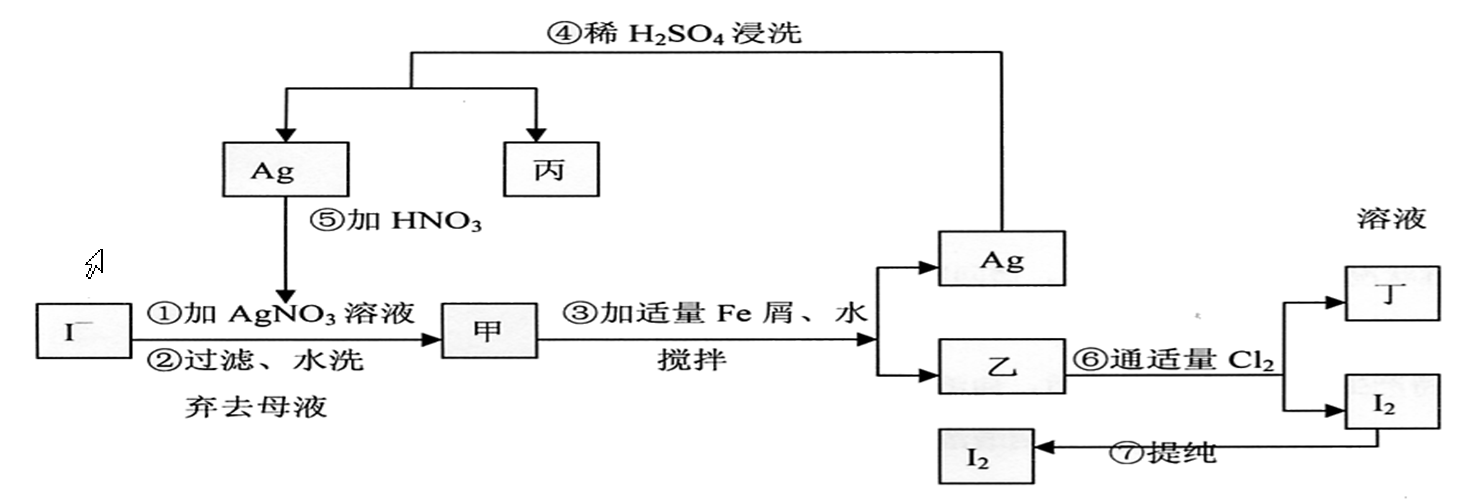
问题一、乙、丁中溶质的分子式:乙(),丁()。
问题二、第④步操作中用稀H2SO4浸洗的目的是()。
A除去未反应的NO3-
B除去未反应的I-
C除去未反应的Fed除去碱性物质
问题三、第⑦步操作可供提纯的两种方法是()和()(不要求写具体步骤)
问题四、实验室检验I2的方法是()。
问题五、甲物质见光易变黑,其原因是(用化学方程式表示)()。
问题六、①中溶解银的硝酸应该用()硝酸(填浓或稀)。原因是()。
A.鉴别软水和硬水——观察颜色
B.鉴别NaOH和NH4NO3两种固体——取样、加水溶解、触摸烧杯外壁
C.除去MnO2中的少量KCl固体——加足量水溶解、过滤、蒸发
D.除去FeSO4溶液中的少量CuSO4——加足量锌粉、充分反应后过滤
A.甲海域较封闭,盐度高
B.乙海域降水较多,盐度低
C.甲海域河流淡水汇入多,盐度低
D.乙海域蒸发较大,盐度低
A.鉴别软水和硬水 观察颜色
B.鉴别NaOH和NH4NO3两种固体 取样、加水溶解、触摸烧杯外壁
C.除去MnO2中的少量KCl固体 加足量水溶解、过滤、蒸发
D.除去FeSO4溶液中的少量CuSO4 加足量锌粉、充分反应后过滤
A.鉴别软水和硬水 实验方案:观察颜色
B.鉴别NaOH和NH4NO3 两种固体 实验方案:取样,加水溶解、触摸烧杯外壁
C.除去MnO2中的少量KCl固体 实验方案:加入适量水溶解、过滤、蒸发
D.除去FeSO4溶液中少量CuSO4 实验方案:加入适量锌粉、充分反应后过滤
A.混合物X中必定含有Na2CO3,不含Al2(SO4)3
B.溶液Z中溶质主要是钠盐,且必含NaHCO3
C.灼烧沉淀Y,可以得到黑色物质
D.往溶液Z中加入Cu粉,若不溶解,说明X中不含FeCl3
A.73.3 %
B.74.4%
C.75.0%
D.76.8%
A.与乙相比, 甲特有的结构是[①]细胞壁、[③]叶绿体、[⑤]液泡
B.甲的⑤内细胞液中溶解着多种物质
C.甲的①能保护和控制物质进出
D.甲、乙都具有的能量转换器是[⑦]线粒体