 更多“酚钠溶液中通入二氧化碳析出苯酚的反应是属于()。”相关的问题
更多“酚钠溶液中通入二氧化碳析出苯酚的反应是属于()。”相关的问题
A.0.51
B.0.45
C.0.15
D.0.13
解释实验现象:
(1)将CO气体通入二氯化钯溶液中,溶液变黑。
(2)将甲硅烷通入KMnO4溶液中,溶液褪色,有棕黑色沉淀和气泡产生。
(3)将CO2气体通入澄清的石灰水中,溶液变浑浊,继续通入至过量后,溶液又变澄清。
(4)Al4C3和水作用有白色沉淀和气体生成。
(5)向SnCl4溶液中滴加Na2S溶液,有沉淀生成,继续加入沉淀又溶解,再以稀盐酸处理此溶液,又析出沉淀。
(6)向氯化汞溶液中滴加SnCl2溶液,先生成白色沉淀,随着SnCl2溶液滴入至过量,沉淀逐渐变灰、变黑。
(7)向Pb(NO3)2溶液中滴加K2CrO4的中性或弱碱性溶液,生成黄色沉淀;而向Pb(NO3)2溶液中滴加K2CrO4的酸性或强碱性溶液,则无沉淀生成。
A.铁栏杆上涂油漆主要是为了防止生锈
B.不能用铁桶配置波尔多液(硫酸铜溶液与石灰乳混合),是因为硫酸铜会腐蚀铁桶
C.海水晒盐没有把海水直接蒸发干,目的是防止海水中的可溶性杂质随氯化钠一起结晶析出
D.实验室探究工业炼铁的反应原理的实验中,先通入CO是为了得到较纯净的铁
A.把氢氧化钠固体放在托盘天平左盘的纸上称量
B.欲除去氢气中混有的氯化氢气体和水蒸气,将气体先通过氢氧化钠溶液,再通过浓硫酸
C.稀释浓硫酸时,将浓硫酸沿着玻璃棒小心地、慢慢地注入到盛水的量筒中
D.欲除去氢氧化钠溶液中混有的氢氧化钙,可向混合溶液中通入二氧化碳气体,然后过滤、蒸发
A.甲醛溶液,甲酚溶液,樟脑苯酚
B.甲醛溶液,间苯二酚,戊二醛
C.甲醛溶液,甲酚溶液,丁香酚
D.甲醛溶液,甲酚溶液,麝香草酚
E.甲酚溶液,甲醛溶液,间苯二酚
推理判断:
(1)无色晶体(A)在电炉高温下与碳反应得到灰黑色单质(B),(B)与浓氢氧化钠溶液共热生成无色气体(C)和物质(D)的溶液。气体(C)可以使灼热的黑色氧化铜变成单质铜。(A)与氢氟酸作用有气体(E)生成,(E)通水中生成白色沉淀(F)和气体(G),(G)与过量反应物(E)化合得(H)的溶液。(H)的溶液与过量氯化钾作用可以结晶出(1)。(A)与碳酸钠共熔生成物质(D),(A)与炭粉共热的体系通氧气有无色液体(J)生成,(J)与水反应可得(F)。
试给出(A),(B),(C),(D),(E),(F),(G),(H),(I)和(J)的化学式,并完成各步的化学反应方程式。
(2)蓝黑色化合物(A)不溶于水,但可溶于稀盐酸生成(B)的溶液,稀释该溶液时,析出白色沉淀(C),酸化时.沉淀溶解。向(B)的溶液中通硫化氢时,生成灰黑色沉淀(D),该沉淀可溶于浓盐酸。(D)与硝酸反应时产生浅黄色沉淀(E),无色气体(F)和化合物(C)的溶液。(F)在空气中迅速变成红棕色。向(G)的溶液中通硫化氢时,生成黄色沉淀(H)。
试给出(A),(B),(C),(D),(E),(F),(G)和(H)的化学式,并完成各步的化学反应方程式。
(3)金属单质(A)与氯气在加热时反应生成无色液体(B),(B)经金属(A)处理转变为固体化合物(C)。向(C)的盐酸溶液中通入硫化氢气体生成灰黑色沉淀(D),(D)不溶于硫化钠溶液,但可溶于过硫化钠溶液形成(E)的溶液。向(E)的溶液中加入盐酸生成黄色沉淀(F),并有气体(G)放出。
试给出(A),(B),(C),(D),(E),(F)和(G)的化学式,并完成各步的化学反应方程式。
(4)红色化合物(A)经稀硝酸处理后得到黑色沉淀物(B)和无色透明溶液,从该溶液中可以结晶出无色品体(C)。晶体(C)加热时放出红棕色气体(D)。(B)在酸性介质中与二价锰离子作用,溶液逐渐变为紫红色,说明有化合物(E)生成。若向(C)的水溶液中滴稀盐酸有白色沉淀(F)生成,(F)不溶于氨水;若向(C)的水溶液中滴碘化钾溶液,则生成黄色沉淀(G);若向(C)的水溶液中滴加氢氧化钠溶液,有白色沉淀(H)生成,氢氧化钠过量则沉淀消失。
试给出(A),(B),(C),(D),(E),(F),(G)和(H)的化学式,并完成各步的化学反应方程式。
(5)物质(A)为黄灰色固体,与水反应得白色沉淀(B)、气体(C)及无色溶液。(B)可以溶于氢氧化钠溶液,若与氧化物(D)作用将生成(E)和水。(B)受热脱水生成(F),经过高温灼烧的(F)既不溶于酸,也不溶于碱,但与焦硫酸钾共熔可得两种能溶于水的化合物,其中一种是(E)。将气体(C)通入硝酸铅溶液得黑色沉淀(G),(G)与臭氧反应转化为白色固体(H)。
试给出(A),(B),(C),(D),(E),(F),(G)和(H)的化学式,并完成各步的化学反应方程式。
A. 生产含水铝硅酸钠(钠硅渣)造成部分氧化铝的损失
B. 含水铝硅酸钠在生产设备和管道上,特别是在换热表面上析出成为结疤,使传热系数严重降低,增加能耗和清理工作
C. 残留在铝酸钠溶液中的二氧化硅在分解时会随同氢氧化铝一起析出,降低了产品质量
D. 大量的钠硅渣的生产增加了赤泥量,可能成为及分散的细悬浮体不利于赤泥的分离和洗涤。
某氮肥厂氨氮废水中的氮元素多以NH和NH3·H2O的形式存在,该废水的处理流程如下:![]()
问题一、过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30℃,通空气将氨赶出并回收。
①用离子方程式表示加NaOH溶液的作用:()。
②用化学平衡原理解释通空气的目的:()。
问题二、过程Ⅱ:在微生物作用的条件下,NH经过两步反应被氧化成NO。两步反应的能量变化示意图如下:
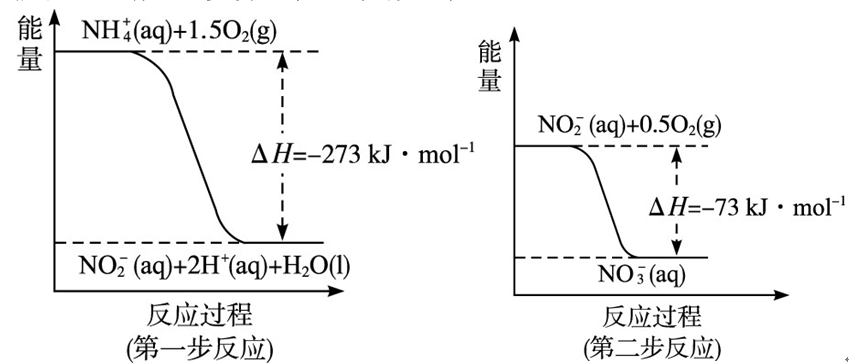
①第一步反应是()反应(选填“放热”或“吸热”),判断依据是()。
②1molNH(aq)全部氧化成NO(aq)的热化学方程式是()。
问题三、过程Ⅲ:一定条件下,向废水中加入CH3OH,将HNO3复原成N2。假设该反应消耗32gCH3OH转移6mol电子,则参加反应的复原剂和氧化剂的物质的量之比是()。


 如果结果不匹配,请
如果结果不匹配,请 
















