 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
为探究锌与足量的稀硫酸的反应速率和生成 H2 的体积时,向反应混合液中加入某种物质,该物质能使反应速率增大,但 H2 的体积减小的是()
A.加入 NH4HSO4 固体
B.加入少量水
C.加入 CH3COONa 固体
D.滴加少量 CuSO4 溶液
 答案
答案
D、滴加少量 CuSO4 溶液
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.加入 NH4HSO4 固体
B.加入少量水
C.加入 CH3COONa 固体
D.滴加少量 CuSO4 溶液
 答案
答案
D、滴加少量 CuSO4 溶液
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“为探究锌与足量的稀硫酸的反应速率和生成 H2 的体积时,向反…”相关的问题
更多“为探究锌与足量的稀硫酸的反应速率和生成 H2 的体积时,向反…”相关的问题
A.决定反应速率的因素只有催化剂
B.食物放在冰箱中会减慢食物变质的速率
C.锌与稀硫酸反应时,加入少量水能加快产生氢气的速率
D.2mol SO2与 1mol O2混合一定能生成2mol SO3
A.①②④
B.②③
C.②④
D.①③④
某化学小组的同学为探究原电池原理,设计如图所示装置,将锌、铜通过导线相连,置于稀硫酸中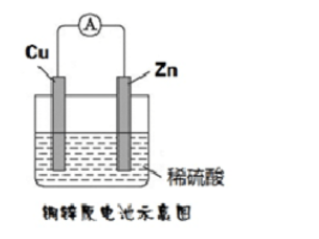 (1)外电路,电子从()极流出。溶液中,阳离子向()极移动。
(1)外电路,电子从()极流出。溶液中,阳离子向()极移动。
(2)若反应过程中有0.2mol电子发生转移,则生成的气体在标准状况下的体积为()。
(3)该小组同学将稀硫酸分别换成下列试剂,电流计仍会偏转的是()(填序号)。
A.无水乙醇
B.醋酸溶液
C.CuSo4溶液
D.苯
(4)实验后同学们经过充分讨论,认为符合某些要求的化学反应都可以通过原电池来实现。下列反应可以设计成原电池的是()(填字母代号)。
A.NaOH+HCl=NaCl+H2O
B.2H2+O2=2H2O
C.Fe+2FeCl3=3FeCl2
D.2H20=2H2↑+2O2↑
A.锌和铜均是金属,锌与稀硫酸反应生成氢气,则铜也能与稀硫酸反应生成氢气
B.气体的溶解度随温度的升高而减小,所以温度越高,氧气的溶解度越小
C.稀盐酸与稀硫酸的化学性质相似,所以实验室可以用大理石与稀硫酸制取二氧化碳
D.催化剂在反应前后质量不变,因此反应前后质量不变的物质一定是催化剂
A.锌与稀硫酸反应有大量气泡产生,放出热量
B.氧化铁与稀盐酸反应,溶液由无色变成浅绿色
C.铁在氧气中剧烈燃烧、火星四射,放出大量的热,生成红色固体
D.一氧化碳还原氧化铜,生成黑色固体
A.能使紫色石蕊溶液变红色
B.能与锌反应生成氢气
C.能与碳酸钠溶液反应生成二氧化碳
D.能与氯化钡溶液反应生成沉淀
A.将乙醇和浓硫酸混合加热,生成的气体先通过足量的水,再通过足量的氢氧化钠溶液,最后通过少量溴水,观察到溴水褪色,证明反应生成了乙烯
B.将某卤代烃和氢氧化钠溶液混合加热,向反应后的溶液中滴加硝酸银溶液,若生成淡黄色沉淀,说明含有溴原子
C.向甲酸溶液中滴加少量新制氢氧化铜悬浊液,加热,未看到砖红色沉淀,说明甲酸分子结构中没有醛基
D.淀粉溶液中加热一定量的稀硫酸,充分加热后再滴加碘水,观察溶液变蓝色,说明淀粉没有水解
铋及其化合物在工业生产中用途广泛,某研究小组用浮选过的辉铋矿(主要成分是Bi2S3,还含少量SiO2等杂质)制备NaBiO3,其流程如下: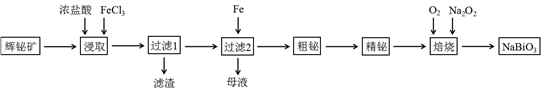 已知:①铋酸钠是一种难溶于水的物质;②水解能力:Bi3+>Fe3+。
已知:①铋酸钠是一种难溶于水的物质;②水解能力:Bi3+>Fe3+。
回答下列问题:
(1)“浸取”时,为了提高浸取速率,可采取的措施有()(任写一条);过滤1的滤渣中的某种主要成分可溶于一种弱酸,写出该反应的化学方程式()。
(2)浸取时加入过量浓盐酸的目的是()。
(3)写出焙烧时生成铋酸钠的化学方程式()。
(4)用H2Dz(双硫腙,二元弱酸)~CCl4络合萃取法可从工业废水中提取金属离子:H2Dz先将金属离子络合成电中性的物质[如Cu(HDz)2等],再用CCl4萃取此络合物。下图是用上述方法处理含有Hg2+、Bi3+、Zn2+的废水时的酸度曲线(E%表示金属离子以络合物形式被萃取分离的百分率)。
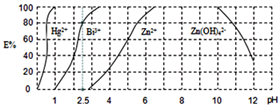 ①当n(Bi3+):n[Bi(HDz)3]=1:4时,废水的pH=()。
①当n(Bi3+):n[Bi(HDz)3]=1:4时,废水的pH=()。
②向萃取后的CCl4中加入足量的NaOH溶液可将Bi(HDz)3中铋元素以氢氧化物的形式沉淀下来,相应的离子方程式为()。
(5)取焙烧得到的NaBiO3样品加入稀硫酸和MnSO4溶液使其完全溶解。已知NaBiO3被还原为Bi3+,Mn2+被氧化成MnO4-,试写出该反应的离子方程式:()。