 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某温度下水的离子积常数为Kw,该温度下,将amol/L的一元酸HA与bmol/L的一元碱BOH等体积混合,可判断该溶液呈中性的依据是()
A.=b
B.混合溶液的pH=7
C.混合溶液中,c(H+)=mol/L
D.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
 答案
答案
C、混合溶液中,c(H+)=mol/L
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.=b
B.混合溶液的pH=7
C.混合溶液中,c(H+)=mol/L
D.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
 答案
答案
C、混合溶液中,c(H+)=mol/L
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某温度下水的离子积常数为Kw,该温度下,将amol/L的一元…”相关的问题
更多“某温度下水的离子积常数为Kw,该温度下,将amol/L的一元…”相关的问题
A.纯净的重水中pD=7
B.1L溶解有0.01mol DCl的重水溶液中,其pD=2
C.1L溶解有0.01mol NaOD的重水溶液中,其pD=12
D.纯净的重水中 ,其c(D+) .c(OD-)>10-14
A.(H+)随着温度升高而降低
B.在35℃时,c(H+)>c(OH—)
C.水的电离程度:(25℃)>(35℃)
D.水的电离是吸热的
A.Na2CO3溶液中c(OH-)大于c(HCO3-)
B.Kw为水的离子积常数,若溶液中c2(OH-)=Kw,溶液pH可能小于7
C.1mol·L-1CH3COOH溶液加水稀释时,溶液中各种离子浓度均减小
D.在CH3COOH溶液中加入碱性固体物质,平衡一定向电离方向移动
A.21:5
B.11:3
C.5:1
D.3:1
高铁酸钾是一种高效的多功能的水处理剂。工业上常采用NaClO氧化法生产,原理为:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O Na2FeO4+2KOH=K2FeO4+2NaOH 主要的生产流程如下: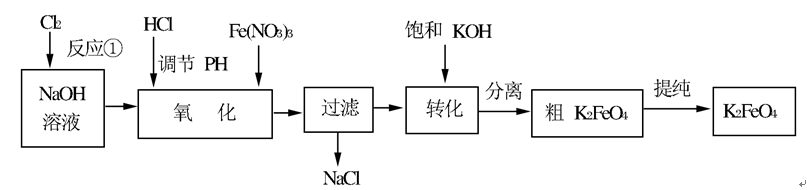 问题一、写出反应①的离子方程式()。
问题一、写出反应①的离子方程式()。
问题二、流程图中“转化”是在某低温下进行的,说明此温度下Ksp(K2FeO4)()Ksp(Na2FeO4)〔填“>”或“<”或“=”〕。
问题三、反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响。
图1为不同的温度下,Fe(NO3)3不同质量浓度对生成率的影响;
图2为一定温度下,Fe(NO3)3质量浓度最正确时,NaClO浓度对K2FeO4生成率的影响
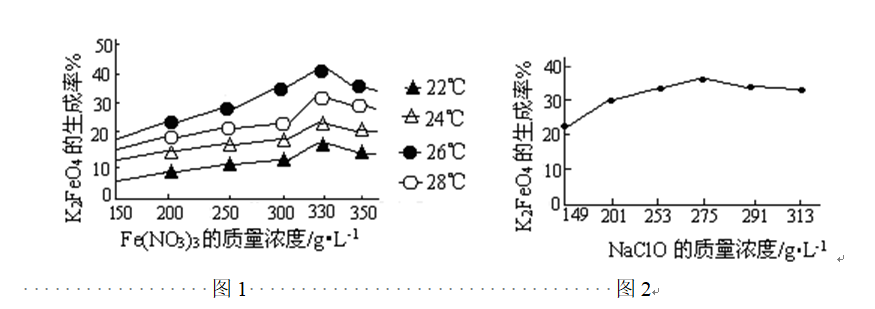
①工业生产中最正确温度为()℃,此时Fe(NO3)3与NaClO两种溶液最正确质量浓度之比为()。
②假设NaClO加入过量,氧化过程中会生成Fe(OH)3,写出该反应的离子方程式:()。假设Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化复原反应生成K3FeO4,此反应的离子方程式:()。
问题四、K2FeO4在水溶液中易水解:
4FeO42—+10H2O 4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用溶液()(填序号)。
4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用溶液()(填序号)。
AH2O
BCH3COONa、异丙醇
CNH4Cl、异丙醇
DFe(NO3)3、异丙醇
A.对于物体由于空气浮力而使质量发生改变的校正
B.玻璃仪器的容积随着温度的改变而改变的校正
C.进行水的密度随着温度的改变而改变的校正
D.进行玻璃仪器的容积随着温度的改变而改变的校正
A.甲分子固定不动,乙分子从很远处向甲靠近到不能再靠近的过程中,分子间的分子势能是先减小后增大
B.一定量的理想气体在体积不变的条件下,吸收热量,内能一定增大,压强必增大
C.已知阿伏伽德罗常数为NA,水的摩尔质量为M,标准状况下水蒸气的密度为(均为国际单位制单位),则1个水分子的体积是
D.自然界进行的涉及热现象的宏观过程都具有方向性,是不可逆的
E.饱和汽压与分子密度有关,与温度无关