 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[判断题]
在抽空密闭的容器中加热NH4C1(s)部分分解成NH3(g)和HCl(g),当系统建立平衡时,其组分数是2()
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在抽空密闭的容器中加热NH4C1(s)部分分解成NH3(g)…”相关的问题
更多“在抽空密闭的容器中加热NH4C1(s)部分分解成NH3(g)…”相关的问题
体积为1dm3的抽空密闭容器中放有0.03458molN2O4(g),发生如下分解反应:

50℃时分解反应的平衡总压为130.0kPa.已知25℃时N2O4(g)和NO2(g)的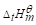
分别为9.16kJ·mol-1和33.18kJ·mol-1.设反应的ΔTGp,m=0.
(1)计算50℃时N2O4(g)的解离度及分解反应的Kθ;
(2)计算100C时反应的Kθ.
A.Na2CO3
B.Na2O2Na2CO3
C.NaOHNa2CO3
D.Na2O2NaOHNa3CO3
g)和H2O(l)。过程放热401.727kJ。求
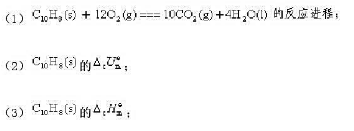
A.2v(NH3) = v(CO2)
B.密闭容器中混合气体的密度不变
C.密闭容器中混合气体的平均摩尔质量不变
D.密闭容器中氨气的体积分数不变
A.反应容器内压强不随时间变化
B.P和S的生成速率相等
C.反应容器内P、Q、R、S四者共存
D.反应容器内总物质的量不随时间而变化
A.0.45 mol/L
B.0.6 mol/L
C.0.9 mol/L
D.1.2 mol/L
A.0.01mol/(L·min)
B.0.6mol/(L·min)
C.0.06mol/(L·s)
D.0.12mol/(L·min)
A.v(NH3)=0.6 mol/(L•min)
B.v(N2)=0.005 mol/(L•s)
C.v(H2)=0.9 mol/(L•min)
D.v(NH3)=0.02 mol/(L•s)
A.1.6 mol
B.2.8 mol
C.2.4 mol
D.1.2 mol