 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
1mol水在100℃,101.325kPa下向真空蒸发,变成100℃,101.325kPa的水蒸气,试计算此过程的△S系,△S环,并判断此过程
1mol水在100℃,101.325kPa下向真空蒸发,变成100℃,101.325kPa的水蒸气,试计算此过程的△S系,△S环,并判断此过程是否自发过程。已知水的蒸发热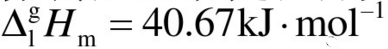 。
。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
1mol水在100℃,101.325kPa下向真空蒸发,变成100℃,101.325kPa的水蒸气,试计算此过程的△S系,△S环,并判断此过程是否自发过程。已知水的蒸发热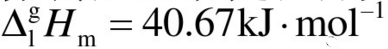 。
。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“1mol水在100℃,101.325kPa下向真空蒸发,变成…”相关的问题
更多“1mol水在100℃,101.325kPa下向真空蒸发,变成…”相关的问题
已知水在100℃,101.325kPa下蒸发热为△hvaQ=2259J·g-1,求1mol,100℃,101.325kPa的水蒸气变为100℃,0.5×101.325kPa的水蒸气的△U,△H,△S,△A与△G。
压力为40.53kPa的水汽末态时的△U及△H。设水蒸气可视为理想气体,液体水的体积相对同样物质的量的水蒸气而言可予忽略。
100℃,标准压强下,1mol液体水的熵值比同温同压下的水蒸气熵值()
A 大
B 小
C 相等
D 无法确定
1mol水蒸气(H2O,g)在100℃,101.325kPa下全部凝结成液态水。求过程的功。
在1cm3、1mol·kg-1的KOH溶液中加入10cm3水,其电导率将
(A) 增大 (B) 减少 (C) 不变 (D) 无法判定
A.1mol/L
B.2mol/L
C.0.1mol/L
D.0.01mol/ml
A.1mol/L的甲酸溶液中c(H+)约为1×10-2 mol/L
B.甲酸能与水以任意比例互溶
C.1mol/L的甲酸溶液10mL恰好与10mL1mol/L的NaOH溶液完全反应
D.在相同条件下,甲酸溶液的导电性比盐酸弱
将1mol H2O(g)从373K、100kPa下,小心等温压缩,在没有灰尘等凝聚中心时,得到了373K、200kPa的介稳水蒸气,但不久介稳水蒸气全变成液态水,即
H2O(g,373K,200kPa)===H2O(l,373K,200kPa)
求该过程的△H、△G和△S。已知在该条件下,水的摩尔汽化热为46.02kJ·mol-1,水的密度为1000kg·m-3。设气体为理想气体,液体体积受压力的影响可忽略不计。