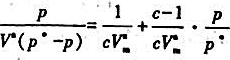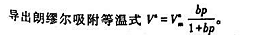题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
60℃时甲醇的饱和蒸气压是834kPa,乙醇的饱和蒸气压是47.0kPa。二者可形成理想液态混合物。若混合物的组成二者
的质量分数各为50%,求60℃时此混合物的平衡蒸气组成,以摩尔分数表示。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
的质量分数各为50%,求60℃时此混合物的平衡蒸气组成,以摩尔分数表示。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“60℃时甲醇的饱和蒸气压是834kPa,乙醇的饱和蒸气压是4…”相关的问题
更多“60℃时甲醇的饱和蒸气压是834kPa,乙醇的饱和蒸气压是4…”相关的问题
甲醇(A)-乙醇(B)溶液(可视为理想溶液)在温度20℃下达到汽液平衡,若液相中甲醇和乙醇各为100g,试计算汽相中甲醇与乙醇的分压以及总压,并计算汽相组成。已知20℃时甲醇的饱和蒸气压为11.83kPa,乙醇为5.93kPa。
A.丙丁烷的临界温度较高,所以容易液化
B.饱和蒸气压随温度变化而变化,丙烷15℃时饱和蒸气压为0.8Mpa,而47℃时为1.6Mpa
C.液化石油气通常气液两相存在,气态比空气重,液态比水轻
D.蒸发潜热小,易挥发,吸热性
假设某气体在固体表面上吸附平衡时的压力p,远远小于该吸附质在相同温度下的饱和蒸气压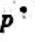 .试由BET公式:
.试由BET公式: