 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知25℃时,氯化银的溶度积为1.8×10-10。求氯化银饱和溶液中Ag+和Cl+的浓度及氯化银的溶解度。已知M(AgCl)=143.4g/mol。
暂无答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知25℃时,氯化银的溶度积为1.8×10-10。求氯化银饱…”相关的问题
更多“已知25℃时,氯化银的溶度积为1.8×10-10。求氯化银饱…”相关的问题
已知氢氟酸的解离平衡常数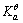 =6.3×10-4,LiF的溶度积常数
=6.3×10-4,LiF的溶度积常数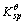 =1.8×10-3,试求LiF在0.5 mol·dm-3氢氟酸中实现沉淀溶解平衡时溶液的pH。
=1.8×10-3,试求LiF在0.5 mol·dm-3氢氟酸中实现沉淀溶解平衡时溶液的pH。
25℃时,实验测得以下三个电池的电动势如下:
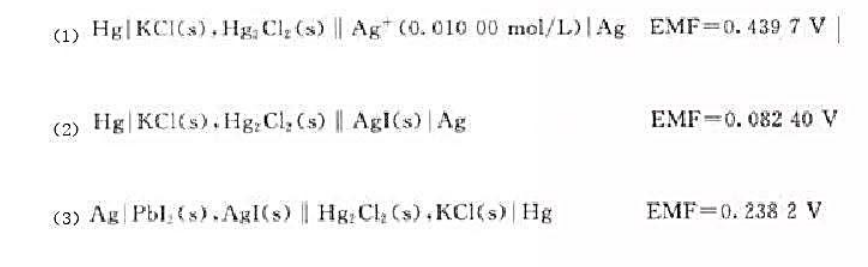
请用实验数据,计算AgI和PbI2的溶度积。已知饱和甘汞电极的电极电位为0.2415V。
体积为1dm3的抽空密闭容器中放有0.03458molN2O4(g),发生如下分解反应:

50℃时分解反应的平衡总压为130.0kPa.已知25℃时N2O4(g)和NO2(g)的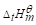
分别为9.16kJ·mol-1和33.18kJ·mol-1.设反应的ΔTGp,m=0.
(1)计算50℃时N2O4(g)的解离度及分解反应的Kθ;
(2)计算100C时反应的Kθ.
A.0.799
B.0.360
C.0.675
D.0.858
已知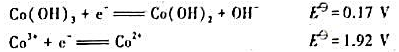
若用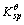 (1)表示Co(OH)3的溶度积常数,
(1)表示Co(OH)3的溶度积常数,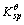 (2)表示Co(OH)2的溶度积常数,试求
(2)表示Co(OH)2的溶度积常数,试求 (1)/
(1)/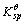 (2)的值。
(2)的值。
25℃时,AgCI的溶度积K =1.71×10-10,试求在饱和水溶液中.AgCI的离子平均活度及离子平均活度系数各为多少?
=1.71×10-10,试求在饱和水溶液中.AgCI的离子平均活度及离子平均活度系数各为多少?
已知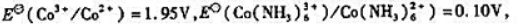
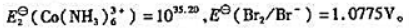
(1)计算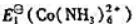 ;
;
(2)写出[Co(NH3)6]2+与Br2(l)反应的离子方程式,计算25℃时该反应的标准平衡常数.
已知25°C时AgBr的活度积Kap=4.88x10-13,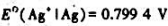 ,
,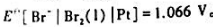 .试计算25℃时
.试计算25℃时
(1)银-溴化银电极的标准电极电势Eθ[Br-|AgBr(s)|Ag];
(2)AgBr(s)的标准摩尔生成吉布斯函数.