 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
煤气化的主要反应为:C(s)+ H2O(g)====CO(g) +H2(g)下列有关叙述错误的是()
A.升高温度,可加快反应速率
B.将块状固体粉碎,可加快反应速率
C.平衡时,反应停止了
D.平衡时,CO的浓度不再改变
 答案
答案
C、平衡时,反应停止了
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.升高温度,可加快反应速率
B.将块状固体粉碎,可加快反应速率
C.平衡时,反应停止了
D.平衡时,CO的浓度不再改变
 答案
答案
C、平衡时,反应停止了
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“煤气化的主要反应为:C(s)+ H2O(g)====CO(g…”相关的问题
更多“煤气化的主要反应为:C(s)+ H2O(g)====CO(g…”相关的问题
A.与深海地区相比,浅海地区水温较高,有利于游离的CO2增多、石灰石沉积
B.与浅海地区相比,深海地区压强大,石灰石岩层易被CO2溶解,沉积少
C.深海地区石灰石岩层的溶解反应为CaCO3(s)+H2O(l)+CO2(aq)===Ca(HCO3)2(aq)
D.海水呈弱碱性,大气中CO2浓度增加,会导致海水中CO浓度增大
A.氢气在负极发生氧化反应
B.供电时的总反应为:2H2+O2=H2O
C.正极:O2+4eˉ+2H2O=4OHˉ
D.电池在工作一段时间电解质溶液浓度不变
A.反应中被氧化和被还原的元素分别为Cu和N
B.反应中氧化剂和还原剂的物质的量之比为3∶2
C.反应中产生0.2mol气体时,转移0.6mol电子
D.该反应中被还原的CuO占参与反应CuO的1/2
电池Ag(s)AgCl(s)]KCl(m)|Hg2Cl2(s)|HIg(I)的电池反应为
Ag(s)+1/2Hg2CI2(s)→AgCl(s)+Hg(I),已知298K时,此电池反应的焓变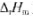 为5435/mol,各物质的规定熵数据为
为5435/mol,各物质的规定熵数据为
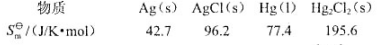 试计算该温度下电池的电动势E及电池电动势的温度系数
试计算该温度下电池的电动势E及电池电动势的温度系数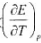
A.升高温度,反应速率减慢
B.当反应达到化学平衡时,υ(正)=υ(逆)=0
C.提高炼铁高炉的高度可减少尾气中CO的浓度
D.某温度下达到平衡时CO的体积分数基本不变
A.v(H2)=v(N2)=v(NH3)
B.v(N2)=3v(H2)
C.v(NH3)=3 v(H2)/2
D.v(H2)=3v(N2)