 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
为检验海带灰浸出液中是否含有I-,可向溶液中加入()
A.淀粉
B.盐酸
C.硝酸酸化的硝酸银
D.CCl4
 答案
答案
C、硝酸酸化的硝酸银
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.淀粉
B.盐酸
C.硝酸酸化的硝酸银
D.CCl4
 答案
答案
C、硝酸酸化的硝酸银
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“为检验海带灰浸出液中是否含有I-,可向溶液中加入()”相关的问题
更多“为检验海带灰浸出液中是否含有I-,可向溶液中加入()”相关的问题
A.要除去氯化镁溶液中少量的氯化铁,可以向溶液中加入适当的氢氧化钠溶液
B.向含有碳酸镁固体的溶液中滴加少许浓盐酸(忽略体积变化),C(CO32-)变小
C.在同浓度的盐酸中,ZnS可溶而CuS不溶,说明CuS的溶解度比ZnS的小
D.向氯化银,溴化银的饱和溶液中加入少量硝酸银,溶液中C(I-):C(Br-)不变
A.海带中碘元素的分离与检验时,需要向海带灰的浸取液中加入稀硫酸和过氧化氢溶液
B.向品红溶液中通入某气体X,溶液变为无色,则X一定是 SO2
C.将含 CO 的氮气通入炽热的氧化铜中除去 CO ,得到纯净的氮气
D.将 Zn 和稀硫酸反应后的废液倒入水槽后再清洗玻璃仪器
A.r-、I-、Cl-
B.r-、Cl-、I-
C.I-、Br-、Cl-
D.l-、I-、Br-
从海带中提取碘单质的工艺流程如下。下列关于海水制碘的说法,不正确的是()。
A.在碘水中加入几滴淀粉溶液,溶液变蓝色
B.实验室在蒸发皿中灼烧干海带,并且用玻璃棒搅拌
C.含I-的滤液中加入稀硫酸和双氧水后,碘元素发生氧化反应
D.碘水加入CCl4得到I2的CCl4溶液,该操作为萃取
A.检验溶液中是否含有Cl-时,用盐酸酸化后再加AgNO3溶液
B.为提高高锰酸钾溶液的氧化能力,用盐酸将高锰酸钾溶液酸化
C.检验溶液中是否含有Fe2+时,用硝酸酸化后,加KSCN溶液
D.检验溶液中是否含有SO42-时,用盐酸酸化后,加BaCl2溶液
工业上利用铅浮渣(主要成分是PbO,Pb,含有少量Ag,CaO和其他不溶于硝酸的杂质)生产硫酸铅和硫化铅纳米粒子,流程如图所示: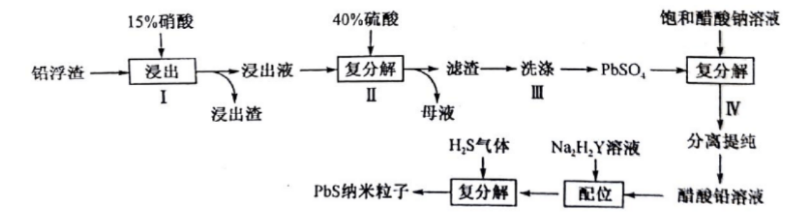 已知:25℃时,
已知:25℃时,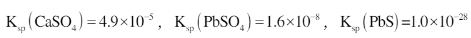 (1)步骤Ⅰ需控制硝酸的用量并使Pb稍有剩余,浸出渣的成分除了不溶于硝酸的杂质和铅外,还主要有()。
(1)步骤Ⅰ需控制硝酸的用量并使Pb稍有剩余,浸出渣的成分除了不溶于硝酸的杂质和铅外,还主要有()。
(2)写出Pb参加反应的化学方程式:()。保持铅剩余的原因是()。
(3)母液的主要成分是()(写化学式),可以循环利用。若母液中残留的SO42-过多,循环利用时可能出现的问题是()。
(4)若浸出液中c(Ca=2+)=0.05mol.L-1,步骤Ⅱ当pb2+完全沉淀后滤渣中是否有CaSO4存在?()(填有或没有)理由是()(通过计算说明)。