 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
在二价铜的配合物中,Cu2+的电子结构常为t2g6,dz22,dx2-y2z1。试根据Jahn—Teller效应解释其结构常
常为四个短键,两个长键,近似为平面正方四配位结构。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在二价铜的配合物中,Cu2+的电子结构常为t2g6,dz22…”相关的问题
更多“在二价铜的配合物中,Cu2+的电子结构常为t2g6,dz22…”相关的问题
A.蓝色沉淀溶解的离子方程式为Cu(OH)2+4NH3·H2O=[Cu(NH3)4]2++2OH-+4H2O
B.NH3极易溶于水是因为氨分子间易形成氢键
C.硫酸四氨合铜在乙醇中的溶解度小于在水中的溶解度
D.NH3比H2O更容易与Cu2+反应形成配合物
和t2g轨道中的分布,并估计它们的磁矩各约为多少(B.M.).指出这些配合物中何者为商自旋排布,何者为低自旋排布.
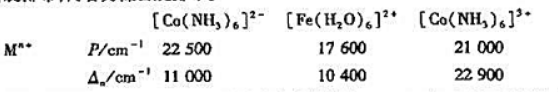
A.NF3分子的空间构型为三角锥形
B.叠氮酸(HN3)是一种弱酸,可部分电离出H+和,则N2O与互为等电子体
C.叠氮化物与Co3+等形成配合物,如[Co(N3)(NH3)5]SO4,则其中钴的配位数为8
D.NaN3与KN3的结构类似,则NaN3的晶格能大于KN3的晶格能
A.只含Fe2+
B.含Cu2+和Fe2+
C.含Cu2+和Fe3+
D.只含Fe3+
A.Ni(CO)4和[Ni(CN)4]2-中,镍元素均是sp3杂化
B.NH3的空间构型为平面三角形
C.O与CN-互为等电子体,其中CO分子内σ键和π键个数之比为1:2
D.Ni2+在形成配合物时,其配位数只能为4
A.可能含有Mg2+
B.一定含有Fe2+、Mg2+
C.一定含有Cu2+
D.一定不含Cu2+