更多“用补偿法测可逆电池电动势,主要是为了在接近()情况下测定电池…”相关的问题
更多“用补偿法测可逆电池电动势,主要是为了在接近()情况下测定电池…”相关的问题
第1题
电池:选择性电极[(a=5.0X10-3mo1/L)]ISCE的电动势为0.386V。计算:(1)用未知活度的溶液代
电池: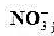 选择性电极[
选择性电极[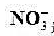 (a=5.0X10-3mo1/L)]ISCE的电动势为0.386V。计算:
(a=5.0X10-3mo1/L)]ISCE的电动势为0.386V。计算:
(1)用未知活度的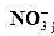 溶液代替已知活度的
溶液代替已知活度的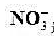 溶液,测得其电动势为0.429v,未知溶液中
溶液,测得其电动势为0.429v,未知溶液中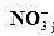 活度为多少?
活度为多少?
(2)若液接电位产生的误差为士0.002V,活度在什么范围内变化?
第2题
溶液pH测定时,常用( )为参比电极,( )为指示电极。若用普通检流计(灵敏度10-9A)测量电池电动势(内阻为103Ω),则pH误差为( )。
溶液pH测定时,常用()为参比电极,()为指示电极。若用普通检流计(灵敏度10-9A)测量电池电动势(内阻为103Ω),则pH误差为()。
点击查看答案
第5题
对于多用电表的使用,下列说法正确的是()
A.在粗略测定电池电动势时,可用直流电压挡直接测量
B.在粗略测定电池内阻时,可用欧姆挡直接测量
C.做电流表使用时与待测电路并联
D.做电压表使用时与待测电路串联
第9题
25℃时,下列电池的电动势为0.518V(忽略液接电位):计算弱酸HA的Ka值.
25℃时,下列电池的电动势为0.518V(忽略液接电位):计算弱酸HA的Ka值.
点击查看答案
25℃时,下列电池的电动势为0.518V(忽略液接电位):
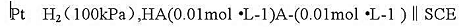
计算弱酸HA的Ka值.
第10题
已知电池(饱和)|Hg2Cl2|Hg的电动势为0.762V,=0.244V,求HA的解离常数(忽略液接电位及离
已知电池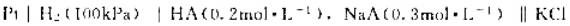 (饱和)|Hg2Cl2|Hg的电动势为0.762V,
(饱和)|Hg2Cl2|Hg的电动势为0.762V,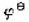 =0.244V,求HA的解离常数(忽略液接电位及离子强度)。
=0.244V,求HA的解离常数(忽略液接电位及离子强度)。
第11题
用下列电池按直接电位法测定草酸根离子浓度。(1)推导出pC2O4与电池电动势之间的关系式(
用下列电池按直接电位法测定草酸根离子浓度。(1)推导出pC2O4与电池电动势之间的关系式(
点击查看答案
用下列电池按直接电位法测定草酸根离子浓度。
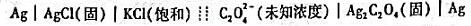
(1)推导出pC2O4与电池电动势之间的关系式
(2)若将一未知浓度的草酸钠溶液置入此电池,在25℃时测得电池电动势为0.402V,Ag-AgCl电极为负极,计算未知溶液的pC2O4。(已知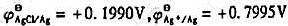 )
)


 如果结果不匹配,请
如果结果不匹配,请