 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列关于SO2、MnO2、SiO2三种物质的叙述中,错误的是()
A.都是氧化物
B.都含有氧元素
C.每个分子中都含有两个氧原子
D.都含有氧分子
 答案
答案
D、都含有氧分子
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.都是氧化物
B.都含有氧元素
C.每个分子中都含有两个氧原子
D.都含有氧分子
 答案
答案
D、都含有氧分子
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列关于SO2、MnO2、SiO2三种物质的叙述中,错误的是…”相关的问题
更多“下列关于SO2、MnO2、SiO2三种物质的叙述中,错误的是…”相关的问题
A.SO2和SO3都属于酸性氧化物
B.KOH和Al(OH)3都属于强碱
C.HClO和HNO3都属于强酸
D.SiO2和Na2SiO3都属于硅酸盐
A.Fe在稀硝酸中发生钝化
B.MnO2和稀盐酸反应制取Cl2
C.SO2与过量氨水反应生成(NH4)2SO3
D.室温下Na与空气中O2反应制取Na2O2
A.Zn粒与稀HNO3反应制备H2
B.用稀HCl和MnO2反应制备Cl2
C.Na2SO3固体与浓H2SO4反应制备SO2
D.加热分解NH4Cl固体制备NH3
锰酸锂离子蓄电池是第二代锂离子动力电池。一种以软锰矿浆(主要成分为MnO2,含少量FeO、A1A、Si02等杂质)为原料制备锰酸锂的流程如下图所示。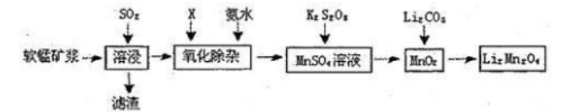 (1)溶浸生产中为提高SO2吸收率可采取的措施有()(填序号)。
(1)溶浸生产中为提高SO2吸收率可采取的措施有()(填序号)。
A、不断搅拌,使SO2和软锰矿浆充分接触
B、增大通入SO2的流速
C、减少软锰矿浆的进入量
D、减小通入SO2的流速
(2)已知:室温下,Ksp[A1(OH)3]=1×10-33,,Ksp[Fe(OH)3]=l×10-39,pH=7.1时Mn(OH)2开始沉淀。氧化除杂时(室温)除去MnSO4液中的Fe3+,Al3+(使其浓度小于1×l06mol.L-1),需调节溶液范围为()。
(3)由硫酸锰与K2S2(V溶液常温下混合一周,慢慢得到球形二氧化锰(MnO2)。请写出发生反应的离子方程式()。
(4)将MnO2和Li2O3按4:1的物质的量比配料,混合搅拌,然后升温至600℃〜750℃,制取产品LiMn2O4。写出该反应的化学方程式()。
(5)锰酸锂可充电电池的总反应为:Li1-xMn2O4+LixC LiMn2O4+C(0
LiMn2O4+C(0
<x<1)
①充电时,电池的阳极反应式为(),若此时转移lmole-,则石墨电极将增重g。
②废旧锰酸锂电池可能残留有单质锂,拆解不当易爆炸、着火,为了安全,对拆解环境的要求是()。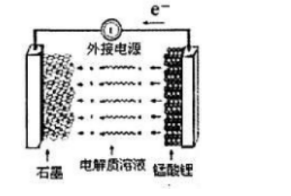
A.S2在水中的溶解度很小,是由于其属于极性分子
B.SO2和NH3均易溶于水,原因之一是它们都是极性分子
C.S2为非极性分子,所以在三种物质中熔、沸点最低
D.NH3在水中溶解度很大只是由于NH3分子为极性分子
下面三个方法都可以用来制氯气:4HCl(浓)+MnO2=MnCl2+Cl2↑+2H2O;4HCl(g)+O2=2Cl2+2H2O(g);2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。 则三个方法中的三种氧化剂由强到弱的顺序是()
A.O2、MnO2、KMnO4
B.KMnO4、MnO2、O2
C.MnO2、KMnO4、O2
D.O2、KMnO4、MnO2