 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
由相同浓度的HA溶液与NaA溶液等体积混合组成的缓冲溶液,若A-的Kb=1.0×10-11,则此缓冲溶液的pH值为()
A.11.0
B.3.0
C.4.0
D.10.0
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.11.0
B.3.0
C.4.0
D.10.0
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“由相同浓度的HA溶液与NaA溶液等体积混合组成的缓冲溶液,若…”相关的问题
更多“由相同浓度的HA溶液与NaA溶液等体积混合组成的缓冲溶液,若…”相关的问题
A.H+浓度相同
B.物质的量浓度相同
C.溶质的质量分数相同
D.pH相同
现有 0.01 molL-1AgNO3溶液和0.01 molL-1KI溶液,欲制AgI溶胶,在下列
四种条件下,能否形成AgI溶胶?为什么?若能形成溶胶,胶粒带何种电荷?
(1)两种溶液等体积混合;
(2)混合时一种溶液体积远超过另一种溶液;
(3)AgNO3溶液体积稍多于KI溶液;
(4)KI溶液体积稍多于AgNO3溶液。
在HA-A缓冲溶液中,A和HA的浓度相等,已知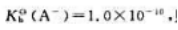
则溶液的pH为().
A、4
B、7
C、10
D、14
有相同物质的量浓度的A、B、C三种一元酸的溶液,已知:
(1)A溶液的pH大于B溶液;
(2)B的钠盐溶液的碱性大于同浓度的C的钠盐溶液。
则这三种酸的酸性由强到弱的顺序是__________。
准确量取30.00ml弱酸,加水稀释至100ml。以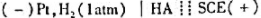 为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
(1)弱酸HA的Ka。
(2)原弱酸HA的浓度。