 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某弱酸HAc的Ka=1(×)10-5,则其0.1mol/L溶液的PH值为:()?
A.1.0
B.2.0
C.3.0
D.3.5
E.5.0
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.1.0
B.2.0
C.3.0
D.3.5
E.5.0
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某弱酸HAc的Ka=1(×)10-5,则其0.1mol/L溶…”相关的问题
更多“某弱酸HAc的Ka=1(×)10-5,则其0.1mol/L溶…”相关的问题
A.HAc-HCI混合溶液
B.NH4Ac溶液
C.HAc-NaAc混合溶液
D.pH=5.00的溶液
A.4.30×10-4mol·dm-3
B.6.25×10-4mol·dm-3
C.1.06×10-3mol·dm-3
D.5.68×10-2mol·dm-3
已知25℃时,醋酸的Kaθ=1.8×10-5,计算: (1)0.10 mol.L-1 HAc溶液的c(H+)、pH、电离度α各为多少? (2)在1.00 L上述溶液中加入0.20 mol固体NaAc后(忽略体积变化),溶液的c(H+)、pH、解离度α分别变为多少?
判断下列溶液的酸碱性并计算其pH值。
(1)0.010mol·L-1弱酸H2O2溶液,已知Ka=1.80×10-12;
(2)0.20mol·L-1NaH2PO4溶液,已知Ka1=7.52×10-3,Ka2=6.23×10-8,Ka3=2.2×10-13;
(3)0.10mol·L-1NaHCO3溶液,已知Ka1=4.3×10-7,Ka2=5.61×10-11;
(4)0.050mol·L-1NaAc溶液,已知Ka=1.76×10-5;
(5)0.10mol·L-1NH4Cl溶液,已知Kb=1.76×10-5。
A.5.0×10-5
B.2.0×10-4
C.1.0×10-4
D.A,B,C均不对
A.HAc(Ka=1.75×10-5)
B.次溴酸(Ka=2.30×10-9)
C.HCN(Ka=6.20×10-10)
D.丙二酸(Ka1=1.42×10-3,Ka2=2.01×10-6)
A.中性
B.无法判断
C.碱性
D.酸性
E.与氯化铵的水解结果一致
欲配制pH=4.5的缓冲溶液,若用HAc和NaAc溶液,则二者的浓度比为( )。
(已知HAc的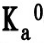 =1.76×10-5)
=1.76×10-5)
(A) 111.8 (B) 3.2/36 (C) 1.8/1 (D) 8/9