 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
在某温度下,可逆反应mA + nB pC + qD的平衡常数为K,下列说法正确的是()
A.K越大,达到平衡时,反应进行的程度越大
B.K越小,达到平衡时,反应物的转化率越大
C.K随反应物浓度的改变而改变
D.K随温度和压强的改变而改变
 答案
答案
A、K越大,达到平衡时,反应进行的程度越大
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.K越大,达到平衡时,反应进行的程度越大
B.K越小,达到平衡时,反应物的转化率越大
C.K随反应物浓度的改变而改变
D.K随温度和压强的改变而改变
 答案
答案
A、K越大,达到平衡时,反应进行的程度越大
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在某温度下,可逆反应mA + nB pC + qD的平衡常数…”相关的问题
更多“在某温度下,可逆反应mA + nB pC + qD的平衡常数…”相关的问题
已知可逆反应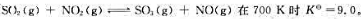 若在此温度下,SO2、NO2、SO2和NO的分压都为50kPa,试通过计算判断反应进行的方向。
若在此温度下,SO2、NO2、SO2和NO的分压都为50kPa,试通过计算判断反应进行的方向。
A.HWS T GW I 02 t5 D45 H-L045 ss nb
B.HWS T GW Ⅵ 02 t5 D45 H-L045 ss nb
C.HRB P GW Ⅰ t10 PC ss nb
D.HD P FW Ⅱ c T10 PD ml
可逆反应 达到化学平衡时:
达到化学平衡时:
(1)升高温度,反应标准平衡常数(),其原因是();
(2)在温度不变的条件下压缩气体的体积而增大压力时,I(g)的解离度().其原因是();
(3)恒容条件下充入N2,I2(g)的解离度(),其原因是()。
(4)恒压条件下充入N2,I2(g)的解离度(),其原因是()。
A.充入NO2
B.升高温度
C.减小压强,扩大容器体积
D.增加压强,缩小容器体积
A.向左进行
B.向右进行
C.处于平衡状态
D.无法确定
A.分离出部分Xe
B.扩大容器体积
C.升高温度
D.分离出部分XeF4