 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列关于溶液的说法中正确的是()
A.均一、稳定的液体都是溶液
B.溶液是均一、稳定的纯净物
C.溶液是无色透明的液体
D.溶液是均一、稳定的混合物
 答案
答案
D、溶液是均一、稳定的混合物
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.均一、稳定的液体都是溶液
B.溶液是均一、稳定的纯净物
C.溶液是无色透明的液体
D.溶液是均一、稳定的混合物
 答案
答案
D、溶液是均一、稳定的混合物
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列关于溶液的说法中正确的是()”相关的问题
更多“下列关于溶液的说法中正确的是()”相关的问题
A.塑料、天然橡胶都是天然高分子化合物
B.乙烯、聚乙烯和苯分子中均含有碳碳双键
C.棉花、羊毛、蚕丝的成分均属于天然纤维素
D.乙酸和乙醇可用碳酸钠溶液加以区别
A.相同浓度的量溶液中c(H+)相同
B.100mL0.1mol/L的两溶液能中和等物质的量的氢氧化钠
C.pH=3的两溶液稀释100倍,pH都为5
D.两溶液中分别加入少量对应的钠盐,c(H+)均明显减小
A.甲烷、乙烷、苯和邻二甲苯均能使酸性KMnO4溶液褪色
B.苯使溴水褪色的原因是苯与溴水发生了加成反应
C.苯与浓硝酸浓硫酸在加热条件下发生反应,反应类型为氧化反应
D.乙炔使溴水褪色与苯在一定条件下与氢气反应,反应类型相同
A.该实验中有两次加入蒸馏水,均是为了析出DNA
B.该实验操作中要多次搅拌,除最后一步未强调方向外,其余均要求单向搅拌
C.该实验中有3次过滤,过滤时使用纱布的层数与滤液或黏稠物有关
D.实验中3次加入浓度为2 mol/L的NaCl溶液,均是为了溶解DNA
A.所有铵盐受热均可以分解,产物均有NH3
B.所有铵盐都易溶于水,所有铵盐中的N均呈-3价
C.NH4Cl溶液中加入NaOH浓溶液共热时反应的离子方程式为NH4++OH-=(加热)NH3↑+H2O
D.NH4Cl和NaCl的固体混合物可用升华法分离
海洋中蕴含丰富的资源,下图涉及多个以海水为原料的生产流程。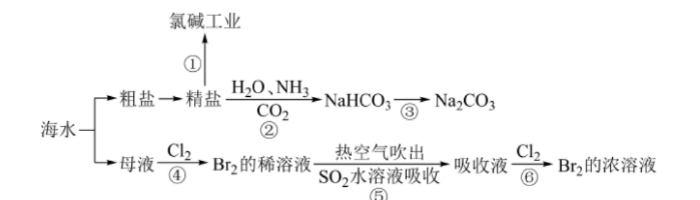 完成下列填空:
完成下列填空:
(1) 步骤①中电解饱和食盐水的化学方程式是()。
(2)工业上用Cl2与KOH(热溶液)制备KClO3,,Cl2+KOH=KCl+KClO3+H2O。配平上述反应方程式,并标出电子转移方向和数目()。
(3)关于卤素的下列说法错误的是()。
A、单质的熔点:Cl2>Br2>I2
B、元素的非金属性:Cl>Br>I
C、单质的氧化性:I2>Br2>Cl2
D、从海洋中获得Cl2,Br2的过程均涉及氧化还原反应
(4)对图中所示生产过程的说法正确的是()。
A、溶解度:NaHCO3>Na2CO3
B、第④⑤⑥步骤中,溴元素均被还原
C、第⑤⑥步骤的目的是进行溴的富集,提高Br2的浓度
D、联碱法与氨碱法相比,NaCl利用率较高,且能耗低
(5)步骤②是在饱和食盐水中先通入NH3再通入CO2,原因是()。
(6)某同学将CO2通入NaOH溶液中,当溶液呈中性时,溶液中浓度最大的微粒是()。
A、c(Na+)B、c(CO32-)C、c(HCO3-)D、c(H+)
A.中性溶液中一定是c(H+)=c(OH-)=1×10-7mol/L
B.向0.1mo1/L的盐酸溶液中加入适量的蒸馏水,则c(H+)、c(OH-)均减少
C.250C时,pH=9的溶液中不可能存在CH3COOH分子
D.250C时,pH=5的溶液中可能存在NH3·H2O分子
A.增大c(CH3COOH),b增大
B.加水稀释,b减小
C.的大小只与温度有关
D.以上说法均不对
A.实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取
B.用乙醇和浓H2SO4制备乙烯时,可用水浴加热控制反应的温度
C.氯离子存在时,铝表面的氧化膜易被破坏,因此含盐腌制品不宜直接放在铝制容器中
D.将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀,表明二者均可使蛋白质变性
A.100g溶液中含氯化钠10g
B.100g水中含氯化钠10g
C.100g溶液中含氯化钠90g
D.100g水中含氯化钠90g
A.Na2CO3溶液中c(OH-)大于c(HCO3-)
B.Kw为水的离子积常数,若溶液中c2(OH-)=Kw,溶液pH可能小于7
C.1mol·L-1CH3COOH溶液加水稀释时,溶液中各种离子浓度均减小
D.在CH3COOH溶液中加入碱性固体物质,平衡一定向电离方向移动