题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知配离子[FeF 5 (H 2 O)] 2- 的磁矩为 5.8B.M.,则该配离子的空间构型为________形,中心离子
已知配离子[FeF 5 (H 2 O)] 2- 的磁矩为 5.8B.M.,则该配离子的空间构型为________形,中心离子 d 电子的排布方式为________,配离子的晶体场稳定化能为________D q ,估计其分裂能与电子成对能的关系为△ o ________P。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知配离子[FeF 5 (H 2 O)] 2- 的磁矩为 5.8B.M.,则该配离子的空间构型为________形,中心离子 d 电子的排布方式为________,配离子的晶体场稳定化能为________D q ,估计其分裂能与电子成对能的关系为△ o ________P。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知配离子[FeF 5 (H 2 O)] 2- 的磁矩为 5…”相关的问题
更多“已知配离子[FeF 5 (H 2 O)] 2- 的磁矩为 5…”相关的问题
已知[Fe(H 2 O) 6 ]] 2+ 的分裂能△ o 为 10400cm -1 ,电子成对能 P 为 17600cm -1 ,可推断该配合物的中心离子 d 轨道排布方式为________,磁矩约为________B.M.,配合物属于________自旋配合物,其晶体场稳定化能为________D q 。
计算在pH=10.0,C(NH3)=0.1mol·dm-3的溶液中Zn2+/Zn电对的条件电极电势(忽略离子强度的影响)。已知锌氨配离子的各级稳定常数为:lgβ1=2.27,lgβ2=4.61,lgβ3=7.01,lgβ4=9.06。
研究发现棕色配位化合物[Fe(NO)(H2O5)]SO4显顺磁性,并测得其磁矩为 3.8μa。
(1)试给出中心离子d电子的排布方式及杂化轨道类型;
(2)[Fe(NO)(H2O5)]SO4中N—O键的键长与自由NO分子中键长相比,
变长还是变短?试简述理由
已知下列配合物的分裂能(△。)和中心离子的电子成对能(P),写出各中心离子的d电子排布式,并估算它们的磁矩各为多少。指出这些配合物中何者为高自旋型,何者为低自旋型?
配离子 (1)[Co(NH3)6]2+(2) [Fe(H2O)6]2+(3)[Co(NH3)6]3+
P/cm-122500 17600 21000
△。/cm-111000 1040O 22900
A.har a[] = "Hello
B.har a[][] = {'H', 'e', 'l', 'l', 'o'}
C.har a[5] = Hello
D.har a[2][5] = {"Hello","world"}
A.一个青蒿素分子由42个原子构成
B.青蒿素的相对分子质量为282
C.H、O元素的质量比为15:22:5
D.青蒿素由3种元素组成
A.ay(H)=ay(N)
B.ay(H)=10^5ay(N)=10^4
C.ay(H)=10^4ay(N)=10^5
D.ay(H)=10%ay(N)=10^2
一氧化氮(NO)分子被美国《科学》杂志命名为1992年明星分子。在无机化学和生物无机化学中,NO是已得到深入研究的分子之一。
(1)写出基态的价电子组态,并回答下列问题:
(a)N原子和O原子间形成什么形式的化学键?
(b)键级多少?
(c)按原子共价半径估算N-O间的键长,并和实验测定值115pm比较。
(d)分子第一电离能比N2是高还是低?说明原因。比O2又如何?
(e)NO+键级是多少?估计其键长。
(D)NO+的伸缩振动波数比NO是大还是小?估计其数值.
(2)若忽略电子的轨道运动对磁矩的贡献,计算NO分子的磁矩。
(3)已知NO红外光谱的两个谱带的波数分别为1876.2cm-1和3724.6cm-1,计算第三泛音带的波数。
(4)NO紫外光电子能谱(HeⅡ线,40.8eV)的一部分示于图C.7.1中,图中的谱带对应于2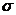 轨道。试解释此能谐分裂为两个谱带(分别对应于3Ⅱ和1Ⅱ态)的原因,并估算从2
轨道。试解释此能谐分裂为两个谱带(分别对应于3Ⅱ和1Ⅱ态)的原因,并估算从2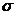 轨道击出的光电子的最大动能。
轨道击出的光电子的最大动能。
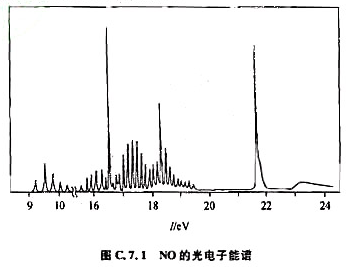
(5)在腌肉时加入NaNO2,产生NO,NO与从蛋白质中解离出来的硫和铁结合生成[Fe4S3(NO)7]-,该离子有抑菌、防腐作用。X射线结构分析表明该离子的结构如图C.7.2所示,请指明该离子所属点群。