 更多“电泳后用纯水()洗的目的是除去杂质离子,防止产生()涂膜弊病…”相关的问题
更多“电泳后用纯水()洗的目的是除去杂质离子,防止产生()涂膜弊病…”相关的问题
从含镍废催化剂中可回收镍,其流程如下: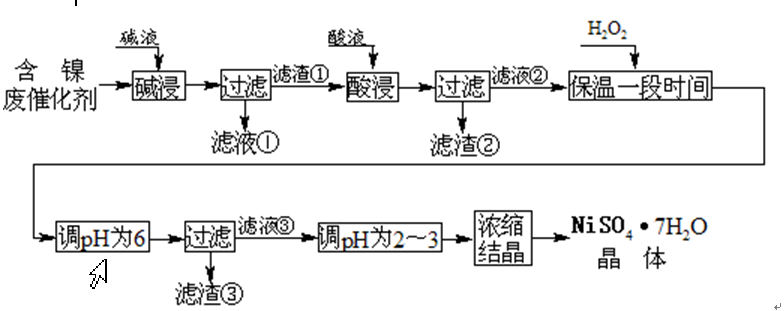 某油脂化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。部分阳离子以氢氧化物形式完全沉淀时的pH如下
某油脂化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。部分阳离子以氢氧化物形式完全沉淀时的pH如下
问题一、碱浸“的目的是除去()。
问题二、“酸浸”时所加入的酸是()(填化学式)。酸浸后,滤液②中可能含有的金属离子是()。
问题三、“调pH为2~3”的目的是()。
问题四、产品晶体中有时会混有少量绿矾(FeSO4•7H2O),可能是由于生产过程中()导致Fe2+未被完全氧化造成的。
问题五、NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料——NiOOH。该反应的离子方程式是()
A.先用水或水一洗涤灵洗,若未洗净,再考虑选择其它洗涤剂洗
B.先用铬酸洗液浸泡除去污染物,然后用氢氧化钾—乙醇液除去油污,再用水一洗涤灵洗洗净
C.先用氢氧化钾一乙醇液除去油污,然后用铬酸洗液浸泡除去污染物,最后用水洗净
D.只能用铬酸洗液浸泡,才能将锥形瓶洗净
A.O(水蒸气): 通过浓硫酸洗气
B.O2(HC濿): 通过饱和 NaHCO3 溶液洗气
C.NaC濿 固体(沙子):溶于水、过滤、洗涤、干燥
D.铁粉(锌粉):加入稀 H2SO4溶液充分反应后过滤
A.HNO3溶液(H2SO4),适量BaCl2溶液,过滤
B.O2(SO2),酸性KMnO4溶液、浓硫酸洗气
C.KNO3晶体(NaCl),蒸馏水,结晶
D.2H5OH(CH3COOH),加足量CaO,蒸馏
A.Zn粉(Fe)——ZnCl2溶液浸泡,过滤
B.碳粉(MnO2)——滴入H2O2溶液,过滤
C.NaCl溶液(Na2SO4)——MgCl2溶液过滤
D.O2(H2O)——通过盛有浓硫酸的洗气瓶
A.Zn粉(Fe):用ZnCl2溶液浸泡,过滤
B.炭粉(MnO2):滴入H2O2溶液,过滤
C.NaCl溶液(Na2SO4):加入适量MgCl2溶液过滤
D.O2(H2O):通过盛有浓H2SO4的洗气瓶


 如果结果不匹配,请
如果结果不匹配,请 
















