 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
25℃时,下列电池的电动势为0.518V(忽略液接电位):计算弱酸HA的Ka值.
25℃时,下列电池的电动势为0.518V(忽略液接电位):
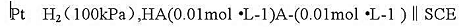
计算弱酸HA的Ka值.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
25℃时,下列电池的电动势为0.518V(忽略液接电位):
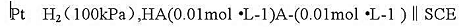
计算弱酸HA的Ka值.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“25℃时,下列电池的电动势为0.518V(忽略液接电位):计…”相关的问题
更多“25℃时,下列电池的电动势为0.518V(忽略液接电位):计…”相关的问题
用下列电池按直接电位法测定草酸根离子浓度。
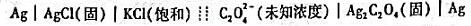
(1)推导出pC2O4与电池电动势之间的关系式
(2)若将一未知浓度的草酸钠溶液置入此电池,在25℃时测得电池电动势为0.402V,Ag-AgCl电极为负极,计算未知溶液的pC2O4。(已知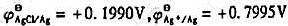 )
)
自发电池: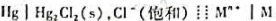 。在25℃时,测得电动势为0.100V,如将Mn+浓度稀释50倍,测得电池电动势为0.050V,此时金属离子的电荷数n是多少?
。在25℃时,测得电动势为0.100V,如将Mn+浓度稀释50倍,测得电池电动势为0.050V,此时金属离子的电荷数n是多少?
25℃时,实验测得以下三个电池的电动势如下:
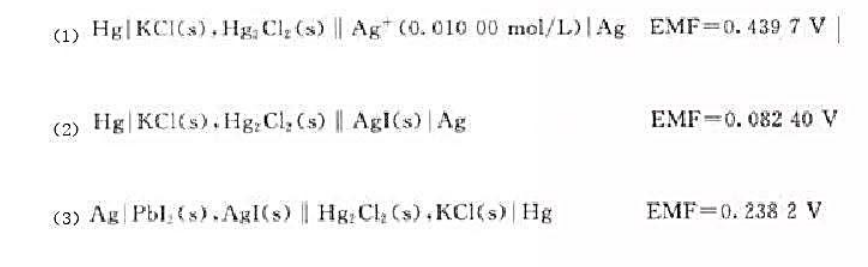
请用实验数据,计算AgI和PbI2的溶度积。已知饱和甘汞电极的电极电位为0.2415V。
A.电对Fe3+/Fe2+做正极
B.反应Fe+2Fe3+=3Fe2+的平衡常数大约为8×1040
C.电池组成式为(-)Fe|Fe2+(c1)||Fe2+(c2),Fe3+(c3)|Pt()
D.电池的标准电动势为0.331V
下列电池的电动势为0.460V。计算反应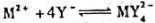 生成的配合物
生成的配合物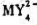 的稳定常数
的稳定常数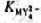 (已知
(已知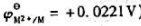 )。
)。
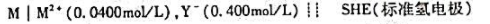
电池:(一)玻璃电极|缓冲溶液(pH=4.03)||饱和甘汞电极(),测得电动势为0.270V,当已知pH的缓冲溶液换成某一未知液时,测得电动势为0.304V,求未知液的pH。
答:
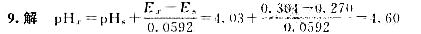
准确量取30.00ml弱酸,加水稀释至100ml。以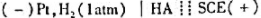 为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
(1)弱酸HA的Ka。
(2)原弱酸HA的浓度。
已知电池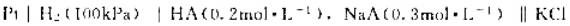 (饱和)|Hg2Cl2|Hg的电动势为0.762V,
(饱和)|Hg2Cl2|Hg的电动势为0.762V,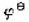 =0.244V,求HA的解离常数(忽略液接电位及离子强度)。
=0.244V,求HA的解离常数(忽略液接电位及离子强度)。
电池: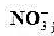 选择性电极[
选择性电极[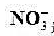 (a=5.0X10-3mo1/L)]ISCE的电动势为0.386V。计算:
(a=5.0X10-3mo1/L)]ISCE的电动势为0.386V。计算:
(1)用未知活度的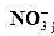 溶液代替已知活度的
溶液代替已知活度的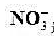 溶液,测得其电动势为0.429v,未知溶液中
溶液,测得其电动势为0.429v,未知溶液中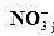 活度为多少?
活度为多少?
(2)若液接电位产生的误差为士0.002V,活度在什么范围内变化?