 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
控制培养基中铵离子浓度防止过高的措施有()
A.低浓度多次补加
B.低速流加
C.添加磷酸镁
D.添加天然沸石
 答案
答案
D、添加天然沸石
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.低浓度多次补加
B.低速流加
C.添加磷酸镁
D.添加天然沸石
 答案
答案
D、添加天然沸石
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“控制培养基中铵离子浓度防止过高的措施有()”相关的问题
更多“控制培养基中铵离子浓度防止过高的措施有()”相关的问题
A.监测浆液Cl-浓度,及时排放浆液,防止Cl-浓缩导致其浓度过高
B.监测浆液pH值。控制pH值范围以防止pH值过低而加速腐蚀
C.保持表面无沉积物或氧化皮,沉积物或氧化皮的聚积会增大点蚀和缝隙腐蚀的危险
D.定期检查,发现问题及时处理
A.监视浆液Cl-浓度,及时排放浆液,防止Cl-浓缩导致其浓度过高
B.监视浆液pH值,控制pH值范围以防止pH值过低而加速腐蚀
C.定期检查,发现问题及时处理
D.运行控制吸收塔浆液中石膏的过饱和度
A.心肌细胞内K+浓度过低,Ca2+浓度过低
B.心肌细胞内K+浓度过高,Ca2+浓度过高
C.心肌细胞内K+浓度过低,Ca2+浓度过高
D.心肌细胞内K+浓度过高,Ca2+浓度过低
A.采用含碱量小于0.6%的水泥
B.在水泥中掺加能抑制碱骨料反应的混合材料
C.使用含钾离子的混凝土外加剂时,须专门试验,严格限制其含量
D.使用含钠离子的混凝土外加剂时,不必限制其含量
E.砂中氯离子含量不得大于6‰
随着工业的迅速发展,产生的废水对水体的污染也日趋严重。通过控制溶液的pH对工业废水中的金属离子进行别离是实际工作中经常使用的方法。下表是常温下金属氢氧化物的Ksp(沉淀溶解平衡常数)和金属离子在某浓度下开始沉淀所需的pH(表中浓度为相应pH时溶液中有关金属离子产生沉淀的最小浓度;当溶液中金属离子浓度小于10-5mol•L-1时通常认为该离子沉淀完全)。 问题一、某厂排出的废水中含有Cu2+和Fe3+,测得其浓度均小于0.1mol•L-l。为除去其中的Fe3+,回收铜,需控制的pH范围是()。
问题一、某厂排出的废水中含有Cu2+和Fe3+,测得其浓度均小于0.1mol•L-l。为除去其中的Fe3+,回收铜,需控制的pH范围是()。
问题二、为了处理含有Cr2O72-酸性溶液的工业废水,采用如下方法:向废水中加人适量NaCl,以Fe为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成排出,从而使废水中铬含量低于排放标准
①Cr2O72-转变为Cr3+的离子方程式为()。
②pH对废水中Cr2072-去除率的影响如右图。你认为电解过程中溶液的pH取值在()范围内对降低废水中的铬含量最有利,请说明理由:()。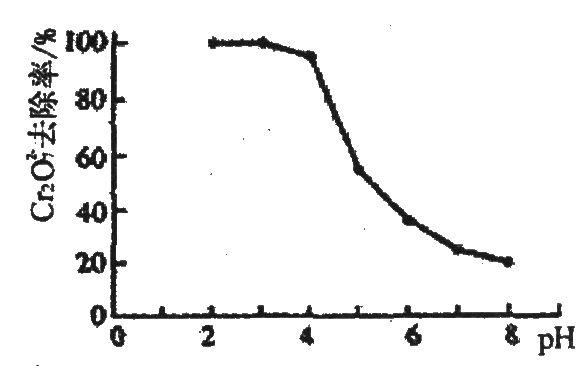
问题三、沉淀转化在生产中也有重要应用。例如,用Na2C03溶液可以将锅炉水垢中的CaS04转化为较疏松而易清除的CaC03,该沉淀转化到达平衡时,其平衡常数K=()。(已知Ksp(CaS04)=9.1x10-6,Ksp(CaC03)=2.8x10-9)
A.葡萄糖和胰岛素同时静脉注射
B.腹膜透析
C.阳离子交换树脂灌肠或口服
D.补充钙剂使细胞外液Ca2+增多
E.补充钠盐使细胞外液Na2+增多