 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列电池的电动势为0.460V。计算反应生成的配合物的稳定常数(已知)。
下列电池的电动势为0.460V。计算反应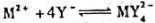 生成的配合物
生成的配合物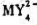 的稳定常数
的稳定常数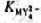 (已知
(已知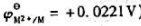 )。
)。
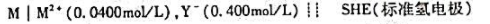
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列电池的电动势为0.460V。计算反应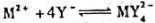 生成的配合物
生成的配合物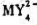 的稳定常数
的稳定常数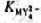 (已知
(已知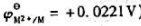 )。
)。
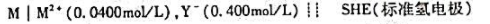
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列电池的电动势为0.460V。计算反应生成的配合物的稳定常…”相关的问题
更多“下列电池的电动势为0.460V。计算反应生成的配合物的稳定常…”相关的问题
A.电对Fe3+/Fe2+做正极
B.反应Fe+2Fe3+=3Fe2+的平衡常数大约为8×1040
C.电池组成式为(-)Fe|Fe2+(c1)||Fe2+(c2),Fe3+(c3)|Pt()
D.电池的标准电动势为0.331V
电池: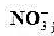 选择性电极[
选择性电极[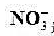 (a=5.0X10-3mo1/L)]ISCE的电动势为0.386V。计算:
(a=5.0X10-3mo1/L)]ISCE的电动势为0.386V。计算:
(1)用未知活度的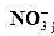 溶液代替已知活度的
溶液代替已知活度的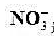 溶液,测得其电动势为0.429v,未知溶液中
溶液,测得其电动势为0.429v,未知溶液中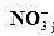 活度为多少?
活度为多少?
(2)若液接电位产生的误差为士0.002V,活度在什么范围内变化?
将电对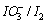 和
和 电对的电势-pH图画在同一直角坐标系中。指出体系中涉及的歧化反应和逆歧化反应发生的具体pH范围。若在298K,pH=11时将所发生的反应以原电池方式完成,试计算原电池的电动势E和电池反应的
电对的电势-pH图画在同一直角坐标系中。指出体系中涉及的歧化反应和逆歧化反应发生的具体pH范围。若在298K,pH=11时将所发生的反应以原电池方式完成,试计算原电池的电动势E和电池反应的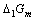 。
。
25℃时,实验测得以下三个电池的电动势如下:
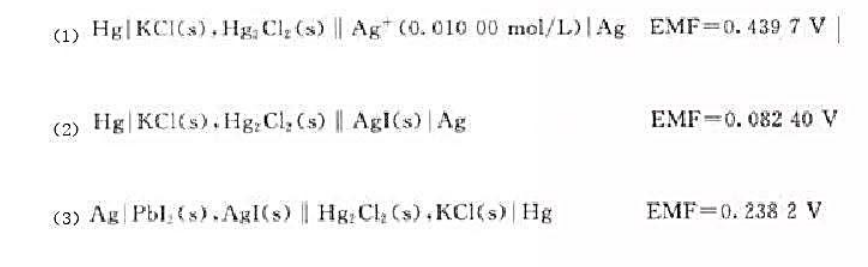
请用实验数据,计算AgI和PbI2的溶度积。已知饱和甘汞电极的电极电位为0.2415V。
电池:(一)玻璃电极|缓冲溶液(pH=4.03)||饱和甘汞电极(),测得电动势为0.270V,当已知pH的缓冲溶液换成某一未知液时,测得电动势为0.304V,求未知液的pH。
答:
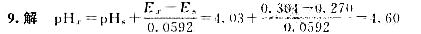
已知电池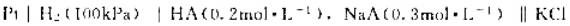 (饱和)|Hg2Cl2|Hg的电动势为0.762V,
(饱和)|Hg2Cl2|Hg的电动势为0.762V,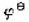 =0.244V,求HA的解离常数(忽略液接电位及离子强度)。
=0.244V,求HA的解离常数(忽略液接电位及离子强度)。
用CaO(s)吸收高炉废气中的SO3气体,其反应方程式为
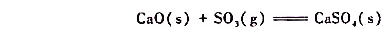
根据下列热力学数据计算该反应373K时的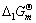 ,以说明反应进行的可能性;并计算反应逆转的温度,进一步说明应用此反应防止S03污染环境的合理性。
,以说明反应进行的可能性;并计算反应逆转的温度,进一步说明应用此反应防止S03污染环境的合理性。

A.醋酸电位滴定是通过测量滴定过程中电池电动势的变化来确定滴定终点
B.滴定终点位于滴定曲线斜率最小处
C.电位滴定中,在化学计量点附近应该每加入0.1~0.2mL滴定剂就测量一次电动势
D.除非要研究整个滴定过程,一般电位滴定只需准确测量和记录化学计量点前后1~2mL电动势变化即可