题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
药物的鉴别方法:取本品1滴,加水50ml,摇匀,分取2ml,加溴化氰试液2m1与2.5%苯胺溶液3ml,摇勾,溶液渐显黄色。该方法鉴别的药物是尼可刹米。()
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“药物的鉴别方法:取本品1滴,加水50ml,摇匀,分取2ml,…”相关的问题
更多“药物的鉴别方法:取本品1滴,加水50ml,摇匀,分取2ml,…”相关的问题
准确量取30.00ml弱酸,加水稀释至100ml。以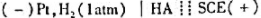 为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
(1)弱酸HA的Ka。
(2)原弱酸HA的浓度。
物)5.00ml,加水稀释至刻度,摇匀,作为对照品溶液。精密量取酊剂溶液7.50ml,置100ml量瓶中,加入正丙醇5.00ml,加水稀释至刻度,摇匀,作为供试液。分别取对照品溶液和供试液1μl注入气相色谱仪,对照品分析时乙醇和丙醇的峰面积分别为1539μV·s和1957μV·s,供试液分析时乙醇和丙醇的峰面积分别为1637μV·s和2012μV·s。计算酊剂中乙醇浓度。
A.试验用试模为金属或硬塑料圆环试模:内径100mm,内部高度25mm
B.试验中可以从砂浆的配合比及加水量计算砂浆的含水率
C.取二次试验结果的平均值作为结果
D.如两个测定值有一个超出平均值的2%,则此试验结果无效
B、病人取左侧卧位
C、液面距肛门40cm
D、肛管插入7~10cm
E、保留溶液10~20min
所用"1、2、3"溶液的成分是A、50%硫酸镁10ml,甘油20ml,温开水30ml
B、50%硫酸镁20ml,甘油40ml,温开水60ml
C、50%硫酸镁40ml,甘油50ml,温开水60ml
D、50%硫酸镁30ml,甘油60ml,温开水90ml
E、50%硫酸镁30ml,甘油50ml,温开水70ml
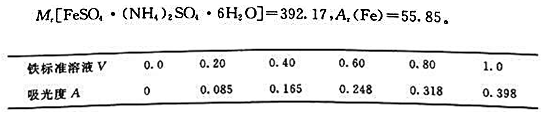
称取0.3511g FeSO4·(NH4)2SO4·6H2O溶于水,加入1:4的H2SO420cm3,定容至500cm3。取体积为V的铁标准溶液置于50cm3容量瓶中,用邻二氮菲显色后加水稀释至刻度,分别测得吸光度列于下表,用表中数据绘制工作曲线。吸取试液5.00cm3,稀释至250cm3,再吸取此稀释液2.00cm3置于50cm3容量瓶中,与绘制工作曲线相同条件下显色后,测得吸光度为0.281,求试液中铁含量ρ(mg·cm-3)。已知