 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列关于溶液的说法错误的是()
A.饱和溶液一定比不饱和溶液要浓
B.溶质可以是固体,也可以是液体或气体
C.糖水、汽水都是溶液
D.所有溶液都是均一、稳定的混合物
 答案
答案
A、饱和溶液一定比不饱和溶液要浓
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.饱和溶液一定比不饱和溶液要浓
B.溶质可以是固体,也可以是液体或气体
C.糖水、汽水都是溶液
D.所有溶液都是均一、稳定的混合物
 答案
答案
A、饱和溶液一定比不饱和溶液要浓
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列关于溶液的说法错误的是()”相关的问题
更多“下列关于溶液的说法错误的是()”相关的问题
A.可以把FeCl3固体直接溶于水制FeCl3溶液
B.热的纯碱溶液去油污效果好
C.l(NO3)3溶液与K2S溶液混合后无明显现象
D.Mg粉投入到饱和NH4Cl溶液中无明显现象
A.冷却或加入硝酸钾固体都能使接近饱和的硝酸钾溶液达到饱和
B.汗水浸湿的衣服晾干后出现白色斑迹,是因为水分蒸发后盐分结晶析出
C.氨水是氨气的水溶液,根据气体溶解度变化的规律,贮存时要阴凉密封
D.氯化钠在20℃时溶解度是36g,则100g的氯化钠溶液中含有氯化钠36g
海洋中蕴含丰富的资源,下图涉及多个以海水为原料的生产流程。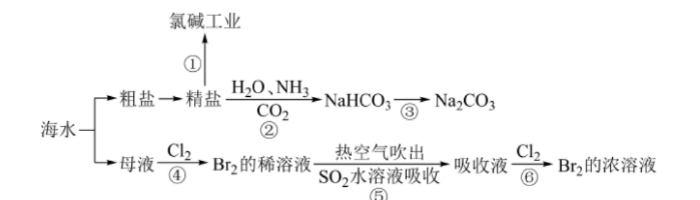 完成下列填空:
完成下列填空:
(1) 步骤①中电解饱和食盐水的化学方程式是()。
(2)工业上用Cl2与KOH(热溶液)制备KClO3,,Cl2+KOH=KCl+KClO3+H2O。配平上述反应方程式,并标出电子转移方向和数目()。
(3)关于卤素的下列说法错误的是()。
A、单质的熔点:Cl2>Br2>I2
B、元素的非金属性:Cl>Br>I
C、单质的氧化性:I2>Br2>Cl2
D、从海洋中获得Cl2,Br2的过程均涉及氧化还原反应
(4)对图中所示生产过程的说法正确的是()。
A、溶解度:NaHCO3>Na2CO3
B、第④⑤⑥步骤中,溴元素均被还原
C、第⑤⑥步骤的目的是进行溴的富集,提高Br2的浓度
D、联碱法与氨碱法相比,NaCl利用率较高,且能耗低
(5)步骤②是在饱和食盐水中先通入NH3再通入CO2,原因是()。
(6)某同学将CO2通入NaOH溶液中,当溶液呈中性时,溶液中浓度最大的微粒是()。
A、c(Na+)B、c(CO32-)C、c(HCO3-)D、c(H+)
A.为了加快反应速率可用饱和食盐水代替水反应
B.此反应是放热反应
C.为了除去杂质气体,除了用硫酸铜外还可用氢氧化钠溶液
D.反应中不需加碎瓷片作沸石
A.在常温和稀溶液中,以下离子交换的顺序为:Al3+、Ca2+、Mg2+、Na+
B.弱酸性阳离子交换树脂只能在碱性溶液中才有较高的交换能力
C.强酸性阳离子交换树脂常采用的活性基团有-SO3H和-COOH
D.吸附达到饱和的阴离子交换树脂可利用高浓度NaOH或NaCl溶液进行再生
A.在一个蒸发器内进行的蒸发操作都单效蒸发
B.蒸发操作是利用了溶液各组分不挥发性不同实现分离的单元操作
C.加热蒸气的饱和温度一定高于同效中二效蒸气的饱和温度
D.蒸发操作时,单位蒸气消耗量随原料液温度的升高而减少
A.该溶液的饱和蒸气压必高于同温度下纯液体A的饱和蒸气压
B.该液体的沸点必低于同样压力下纯液体A的沸点
C.该液体的凝固点必低于同样压力下纯液体A的凝固点(溶液凝固时析出纯固态A)
D.该溶液的渗透压为负值
A.苯的分子式是C6H6,不能使酸性KMnO4溶液褪色,属于饱和烃
B.从苯的凯库勒式看,分子中含有双键,所以属于烯烃
C.在催化剂作用下,苯与液溴反应生成溴苯,发生加成反应
D.苯分子为平面正六边形结构,6个碳原子之间的键完全相同
A.在饱和溶液中,晶核是处于一种形成—溶解—再形成的动态平衡之中,只有达到一定的过饱和度以后,晶核才能够稳定存在
B.要获得结晶过程所必需的驱动力,一定要过冷
C.晶体长大的条件是要求液相不断地向晶体扩散供应原子,晶体表面能够不断而牢靠地接纳这些原子
D.溶液浓度达到饱和溶解度时,晶体便可析出
A.X的单质是人类将太阳能转化为电能的常用材料
B.Y元素可以形成多种含氧酸
C.x元素在自然界中只有化合态没有游离态
D.
W与Z形成的化合物与饱和NaCL溶液的反应要选用如图装置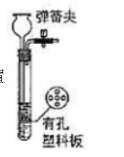
A.在侯氏制碱工业中,向饱和氯化钠溶液中先通二氧化碳,后通氨气
B.在硫酸工业、合成氨工业、硝酸工业中,皆采用循环操作提高原料利用率
C.在氯碱工业,电解槽被离子交换膜隔成阴极室和阳极室
D.工业上采用电解熔融氯化铝的方法制取金属铝
E.石油裂化属于化学变化,主要目的是为了获得短链不饱和气态烃